NEWS
新闻资讯
|
客户文章 | Nature Commun ATAC-seq助力揭示禾谷镰刀菌硝化应激反应机制
发表单位:浙江大学 发表日期:2021年5月6日 期 刊:Nature Commun(IF:17.694) 2021年5月6日,浙江大学农业与生物技术学院马中华教授团队在期刊Nature Commun(IF:17.694)发表题为“Interplay of two transcription factors for recruitment of the chromatin remodeling complex modulates fungal nitrosative stress response”的研究论文。该研究发现FgAreB是谷类作物真菌病原体禾谷镰刀菌(Fusarium graminearum) NS应答的调节因子。FgAreB作为一种先锋转录因子,在NS应答相关基因的启动子上募集染色质重塑复合物SWI/SNF,从而促进其转录。此外,作者还发现一个转录抑制因子(FgIxr1)与SWI/SNF复合物竞争,从而与FgAreB结合,并负向调节NS应答。爱基百客为该研究提供ATAC-seq的技术支持。
研究背景 一氧化氮(NO)是一种在微生物和植物等生物系统中具有高度扩散和反应性的信号分子,可调节动植物的免疫应答。此外,由NO衍生的活性氮可以通过与微生物细胞组分反应而表现出抗菌活性,从而导致病原菌的硝化应激(NS)。小麦组织中NO爆发抑制了禾谷镰刀菌(以下简称Fg)的生长,禾谷镰刀菌是全球范围内严重危害谷类作物的镰刀菌头疫病的主要致病因子。 研究思路
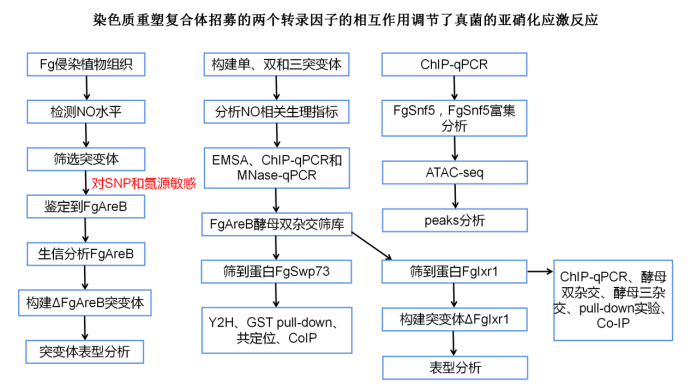
研究结果 1. Fg感染引起植物组织NO爆发。 为了了解NO在宿主防御病原体入侵中的作用,作者首先利用NO敏感荧光探针DAF-FM DA(diaminofluorescein-FM diacetate)测定了禾谷镰刀菌(Fg)侵染后小麦胚轴和玉米须的NO产量。如图1a,在接受禾谷镰刀菌分生孢子或菌丝侵染24h后可以在小麦胚轴或玉米须观察到丰富的NO。这些结果表明,Fg感染可引起宿主组织中NO爆发。 为了确定NO爆发对真菌生长发育的影响,作者用NO供体硝普钠(SNP)处理野生型菌株PH-1。SNP在10 mM时显著诱导NO积累,在2 mM时则没有(图1b),还能抑制菌丝生长(图1c),分生孢子和子囊壳的产生。在含氮培养基(PDA、MM、PDB和YEPD)中,10 mM SNP对Fg菌丝生长和真菌生物量有抑制作用。这些结果表明,诱导NO积累的10mM SNP抑制Fg生长发育。
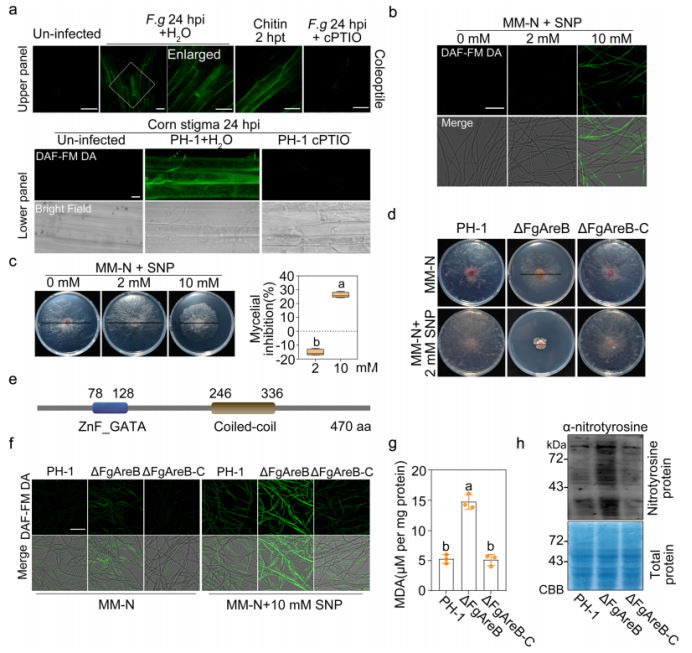
图1 FgAreB介导禾谷镰刀菌氮胁迫的反应 2. FgAreB是Fg中NS反应的调节因子。 为了识别真菌中响应NS反应的调节器,作者筛选了超过1500个靶向SNP敏感的Fg基因缺失突变体,并且鉴定到一个在FGSG_16452位点的突变体;与野生型PH-1菌比较这个突变体对2mM的SNP和各种氮源表现出大幅增加的敏感性(图1 d)。FGSG_16452位点预测编码一个470氨基酸的蛋白,它与构巢曲霉菌的AreB有44.4%的一致性。因此,FGSG_16452此后被指定为FgAreB。FgAreB含有一个典型的锌指GATA结合区域(图1 e),它在许多其他真菌中都是保守的。 Fg包含5个典型的GATA转录因子:FgAreB、FgAreA、FgSreA、FgWC1和 FgWC2。早先研究表明FgWC1和 FgWC2突变没有导致表型变化。作者因此检测了FgAreA和FgSreA突变体对2mM SNP的敏感性,它们皆没有敏感性。这暗示FgAreB可能是Fg中唯一响应NS的GATA型转录因子。为了证实GATA结合域在FgAreB中的作用,作者首先构建了FgAreB缺失突变体(ΔFgAreB)。实验结果表明GATA结构域对FgAreB功能是必须的,但是它对其定位不是必不可少的。 为了进一步验证FgAreB与NS应答的关联,作者测定了NO在ΔFgAreB中的积累。显微镜检查显示ΔFgAreB的NO积累量远高于生长在MM-N培养或没有SNP和各种氮源的培养基上的野生型菌株(图1 f)。表型分析显示ΔFgAreB在分生孢子中严重受损,无法产生外胚层,与野生型PH-1用10 mM SNP处理的表型类似。此外,ΔFgAreB突变体含有丙二醛水平高于用10mM SNP处理的野生型菌PH-1(图1g)和硝基酪氨酸(图1h),这两个都是NS反应的标记物。总之,这些结果暗示FgAreB参与调控Fg中的NS反应。 3. FgAreB可调控Fg中NS应答基因的转录。 此前研究表明,五组NS应答基因负责消除真菌中的NO,比如黄素血红蛋白(FHB,flavohaemoglobins)、S-亚硝基谷胱甘肽还原酶(GSNOR)、P450 一氧化氮还原酶(NOR)、胆色素原脱氨酶(HEMC)和nitrosothionein。BLASTp分析显示Fg含有5个NS响应基因,比如FgFHB1、FgFHB2、FgGSNOR、FgNOR和FgHEMC。除了FgHEMC,4个基因(FgFHB1、FgFHB2、FgGSNOR和FgNOR)在野生型菌中受到10mM SNP的诱导表达,但ΔFgAreB突变体没有,暗示FgAreB调控这4个NS响应基因的转录。 为了阐明这些FgAreB-依赖的NS应答基因是否在基因上参与消除NS,作者构建了这些基因的单、双和三重突变体。作者发现两个三突变体ΔFgNSR1(ΔFgFHB1-FHB2-GSNOR)和ΔFgNSR2(ΔFgFHB1-GSNOR-NOR)对2mM SNP和各种氮源的敏感性显著提高(图2b)。此外,与野生型比较三重突变体积累了更高水平的NO(图2c)、硝基酪氨酸(图2d)和丙二醛(图2e)。这些结果表明FgFHB1、FgFHB2、FgGSNOR、FgNOR参与消除Fg中的NS。生物信息学分析显示这四个基因的启动子包含推定的FgAreB结合顺式元件(图2f)。EMSA实验结果暗示FgAreB在体外特异地结合顺式元件。ChIP-qPCR实验显示在互补菌株中FgAreB-GFP在4个NS响应基因启动子上显著富集,但不在FgHEMC上富集。 为了进一步探索FgAreB是否在缺乏NS的情况下富集包裹核小体DNA的启动子区域,作者在没用SNP处理的野生型菌中进行MNase-qPCR实验。结果显示含有FgGSNOR的FgAreB结合顺式元件(- 380 ~ - 220)的启动子区包裹在一个核小体上(图2h),暗示FgAreB能够在核小体包裹处DNA区域富集。这些结果表明FgAreB能够富集在核小体包裹的DNA区域。
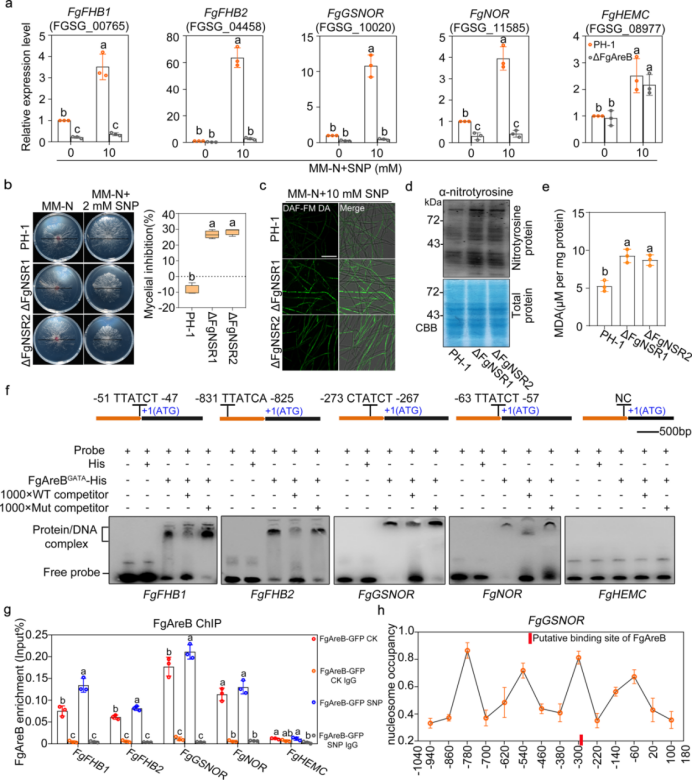
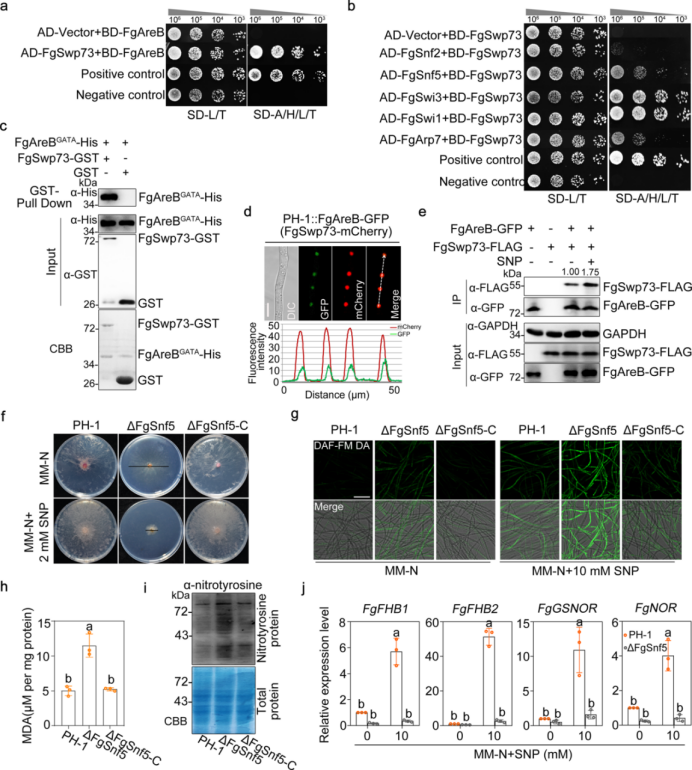
图2 FgAreB调节禾谷镰刀菌的硝化应激反应基因 4. FgAreB通过与FgSwp73直接相互作用与SWI/SNF复合物关联,介导Fg对NS的应答。 为了进一步阐明FgAreB对NS响应的调控机制,作者以Fg cDNA文库为猎物,FgAreB为诱饵,进行酵母双杂交(Y2H)筛库,筛选FgAreB潜在的相作蛋白。在筛选过程中共获得51个假定的FgAreB相互作用蛋白。其中FgSwp73,酿酒酵母Swp73的同系物,是SWI/SNF染色质重塑复合物的核心成分。利用酵母SWI/SNF复合物的亚基进行BLASTp搜索,在Fg中发现了10个SWI/SNF亚基。 Y2H分析显示FgAreB只与FgSwp73相互作用,而与该复合物的其他亚基不相互作用(图3a),而FgSwp73与 FgSnf2、FgSnf5、FgSwi3、FgSwi1和FgArp7互作(图3b)。这些结果表明,FgAreB极有可能通过与FgSwp73相互作用与SWI/SNF复合物关联。此外,通过一系列截短FgAreB的Y2H实验和GST-pull-down试验表明,FgAreB的GATA结构域对其与FgSwp73的相互作用至关重要(图3c)。此外,蛋白质亚细胞定位实验表明FgAreB与SWI/SNF核心亚FgSwp73、FgSnf2和FgSnf5共定位(图3d)。Co-IP实验进一步证实在体内FgAreB与FgSwp73、FgSnf2和FgSnf5互作,它们的互作关系在SNP处理后得到加强(图3e)。总之,这些结果暗示FgAre通过与FgSwp73直接互作关联SWI/SNF复合物。 为了探索FgAreB与SWI/SNF复合物的遗传关联,作者尝试构建每个SWI/SNF亚基的缺失突变体。10个亚基中,6个亚基(FgSwi3、FgSwi1、FgArp9、FgSwp82、FgSnf5和FgTaf14)成功去除,而剩余4个亚基(FgSwp73、FgArp7、FgSnf6和FgSnf2)没有去除,暗示这4个亚基可能对Fg生长所必须。表型分析表明,FgSnf5突变体对2mm SNP和各种氮源的敏感性显著提高(图3f),而FgArp9突变体对SNP敏感。对FgSnf5突变体的进一步鉴定表明,与野生型比较该突变体积累了更高水平的NO(图3g)、丙二醛(图3h)和nitrotyrosine(图3i)。突变体中4个NS应答基因也显著下调。ChIP-qPCR结果显示,SNP处理可促进这些基因启动子处FgSnf5-GFP的富集(图4a)。这些结果表明SWI/SNF复合物至少部分通过调节NS应答基因的转录调控NS应激反应。
图3 FgAreB与SWI/SNF复合物共同调控NS应答基因的转录 5. FgAreB通过招募SWI/SNF复合物调节染色质可及性。 既然SNP处理可以增强FgAreB与SWI/SNF复合物的关联,作者推测FgAreB可能将该复合物招募到NS应答基因的启动子并激活其转录。为了验证这一假设,作者利用ChIP-qPCR分析衡量FgSnf5在FgAreB缺失突变体中NS响应基因启动子上的占有情况。SNP处理显著促进了野生型菌株(PH-1::FgSnf5-GFP)NS应答基因启动子上FgSnf5-GFP的富集,但在ΔFgAreB菌株中没有,这暗示FgSnf5的富集大大地依赖于FgAreB(图4a)。相反,FgAreB-GFP在NS响应基因启动子上的富集不受FgSnf5和SNP处理的影响(图4b;图2g)。此外,ChIP-qPCR和MNase-qPCR实验显示不管是否用SNP处理在ΔFgAreB和ΔFgSnf5突变体中在FgGSNOR启动子FgAreB结合位点上的核小体占有率高于野生型菌朱PH-1(图4c,d),这表明FgGSNOR启动子上的核小体在没有FgAreB或FgSnf5的情况下无法有效退出。此外,FgAreB或FgSnf5基因不影响彼此的转录。这些结果表明FgAreB可能是将SWI/SNF复合物招募到NS应答基因启动子的先锋TF。 考虑到ΔFgAreB和ΔFgSnf5的生长缺陷比三重突变体ΔFgNSR1和ΔFgNSR2严重得多,作者认为,除了NS反应外,FgAreB和FgSnf5可能还参与了Fg其他功能的调控。生长在传统培养基PDB中的ΔFgAreB和ΔFgSnf5突变体RNA-seq数据反映FgAreB和FgSnf5共激活657个基因,共抑制1431个基因(图4e)。与RT-PCR结果一致,在这两个ΔFgAreB和ΔFgSnf5突变体中NS响应基因FgFHB1、FgFHB2和FgNOR显著下调。下调基因的GO富集分析暗示FgAreB和FgSnf5参与一些关键代谢过程,包括ADP、嘌呤核苷和核苷、吡啶核苷、单糖,这可能部分解释ΔFgAreB和ΔFgSnf5突变体严重生长缺陷。 为了进一步验证FgSnf5和FgAreB在调控染色质可及性的作用,作者利用ATAC-seq技术构建了染色质景观图谱。如图4f,与野生型菌株比较,FgAreB或FgSnf5缺失分别导致2050或1236个不可进入genome peaks。1051个peaks由FgAreB和FgSnf5共调控,在ΔFgSnf5突变体中超过83%不可及peaks在ΔFgAreB中也不可及(图4f)。另外一方面,与野生菌株相比,ΔFgAreB和ΔFgSnf5突变体分别增加了1494和2063个可及peaks。其中802个增加的可及peaks由由FgAreB和FgSnf5共调控(图4f),意味着ΔFgSnf5突变体中38.9%增加可及peaks在ΔFgAreB突变体中也开放。以峰为中心的热图也表明,ΔFgAreB中染色质不可接近的峰值与ΔFgSnf5的高度重叠(图4g,h)。综上所述,这些结果表明FgAreB与FgSnf5协同主要调节染色质可及性,尽管它们也在调控染色质不可及性方面发挥作用。
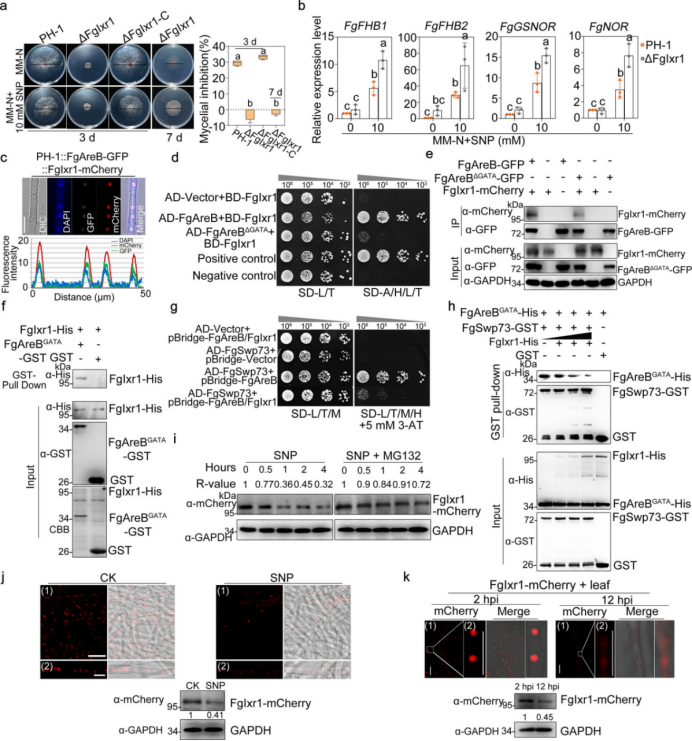
图4 FgAreB通过激活SWI/SNF复合物来调控基因表达和染色质可及性 6. FgIxr1与FgAreB竞争性相互作用,阻止FgAreB与SWI/SNF复合物相互作用。 在cDNA文库筛选实验中,筛到FgAreB另外一个互作蛋白——FgIxr1,是酿酒酵母中的一个同源基因,编码一个转录抑制因子。表型分析显示FgIxr1突变体(ΔFgIxr1)与野生型相比,对10 mM SNP的抗性增强(图5a)。在ΔFgIxr1突变体响应SNP处理,NS响应基因的转录水平高于野生型(图5b),暗示FgIxr1可能负调控NS反应。ChIP-qPCR检测结果显示,SNP处理后,FgGSNOR基因启动子上FgIxr1-GFP富集显著减少。 为了阐明FgIxr1对NS应答基因的转录抑制机制,作者首先检查了Fglxr1的定位,且发现在MM-N条件下FgIxr1-mCherry与FgAreB-GFP共定位在核内,它们之间的互作关系由酵母双杂交和Co-IP实验确定(图5d,e)。FgAreB的GATA结构域对这个互作非常关键(图5d-f),因为将FgAreB截短去掉GATA结构域与FgIxr1的互作显著减少(图5d,e)。考虑FgAreB的GATA结构域对其与FgSwp73的互作非常关键,作者推测在与FgAreB的互作中FgIxr1可能与FgSwp73竞争。作者进行了酵母双杂交、酵母三杂交、pull-down实验、Co-IP等证实了这一推测。为了进一步了解FgIxr1调控NS应答基因转录的机制,我们测定了FgIxr1在SNP处理下的转录和翻译水平。作者利用RT-PCR、荧光显微镜等手段发现SNP处理可能促进FgIxr1的降解。
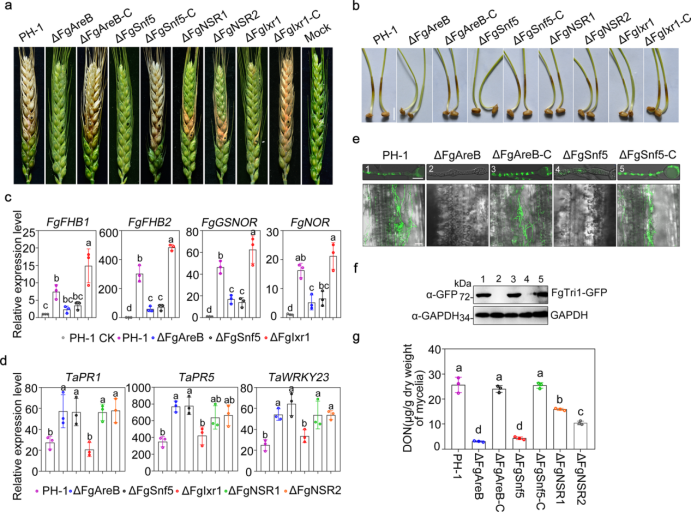
图5 FgIxr1和FgSwp73与FgAreB相互竞争 7. FgAreB和FgSnf5是禾谷镰刀菌毒力所必需的。 为了确定病原真菌的NS反应是否对毒力有重要影响,作者检测了ΔFgAreB、ΔFgSnf5、 ΔFgNSR1、ΔFgNSR2和ΔFgIxr1对开花小麦穗和小麦胚芽鞘的毒力水平。两个ΔFgAreB和ΔFgSnf5对小麦穗和胚芽鞘无致病作用;而ΔFgIxr1、ΔFgNSR1和ΔFgNSR2均显示毒性降低(图6a,b)。此外,由于禾谷镰刀菌的NS应激基因负责抵抗NS,在真菌侵染12小时时这些基因在PH-1和ΔFgIxr1中的表达高于那些ΔFgAreB和ΔFgAreB(图6c)。 之前的研究表明NO也能激活植物防御相关基因的转录,因此作者检测了侵染后小麦幼苗叶片中防御相关基因的表达。用ΔFgAreB、ΔFgSnf5、ΔFgNSR1和ΔFgNSR2突变体侵染后小麦细胞的基因TaPR1、TaPR5和TaWRKY23表达高于那些用PH-1和ΔFgIxr1(图6d)。作者还研究了突变体的毒素形成。ΔFgAreB和ΔFgSnf5在TBI培养基和小麦组织上不能形成正常的绿色球形和新月形毒素体,而PH-1和互补菌株可以形成毒素体(图6e)。ΔFgAreB和ΔFgSnf5突变体中FgTri1-GFP的GFP信号无法监测到(图6f),与野生型比较ΔFgAreB、ΔFgSnf5、ΔFgNSR1和ΔFgNSR2突变体的DON产量明显减少(图6g)。总之,这些结果暗示对NS的敏感性增加和DON产量的减少可能有助于减弱ΔFgAreB、ΔFgSnf5、ΔFgNSR1和 ΔFgNSR2对小麦的毒性。
图6 FgAreB、FgSnf5和FgNSRs有助于禾谷镰刀菌的毒力 总结在该研究中,作者发现FgAreB通过招募SWI/SNF复合物到靶基因启动子参与调节NS应答,作者也发现FgAreB负调控Fg中许多基因的转录。将目前的发现扩展到其他子囊菌,它肯定会为真菌中氮调节的转录机制和进化提供有趣的见解。 爱基百客有丰富的表观组学经验,欢迎有相关需求的老师前来咨询。 往期推荐: 客户文章 | 12分+,ChIP-seq助力多发性骨髓瘤骨髓血管生成关键因子的发现 客户文章 | ChIP-seq揭示了全局调控因子Vfr调控生物防治剂假单胞菌FD6的新见解 客户文章 | ATAC-Seq 首次揭示大豆疫霉菌(卵菌)基因组开放染色质和顺式作用元件景观 文献下载
|