NEWS
新闻资讯
|
文献解读 | 外泌体circLPAR1通过METTL3-eIF3h相互作用抑制BRD4在结直肠癌诊断和肿瘤发生中发挥作用前期我们通过一篇综述表明了外泌体circRNA在癌症/肿瘤监测、治疗中的重要性,本次向大家展示这篇来自Molecular cancer(IF=27.401)的文献是如何利用表观技术手段对肿瘤外泌体circRNA进行研究的,以期能够为各位老师提供对应的研究思路。
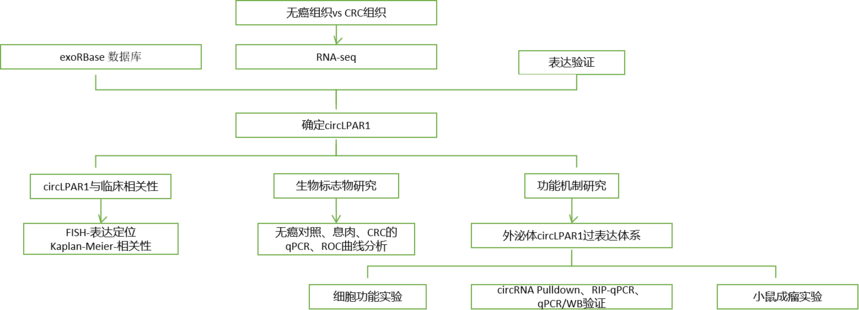
文章标题:Exosomal circLPAR1 functions in colorectal cancer diagnosis and tumorigenesis through suppressing BRD4 via METTL3–eIF3h interaction 研究背景 结直肠癌已成为消化系统最常见的恶性肿瘤之一,到2020年,全球估计有超过190万例新发结直肠癌病例和935,000例死亡。近年来,我国结直肠癌的发病率和死亡率居高不下。尽管一些方法已应用于临床,包括结肠镜检查、乙状结肠镜检查和基于粪便的检测,但结直肠癌的早期发现和诊断仍然具有挑战性。因此,迫切需要鉴定结直肠癌的新型生物标志物。外泌体已成为多种癌症的重要生物标志物,并含有丰富的环状RNA(circRNA)。然而,外泌体circRNA用于诊断的潜力及其在结直肠癌(CRC)中的分子作用机制仍不清楚。 研究技术 RNA-seq;circRNA Pulldown;蛋白组学分析;RIP-qPCR;动物实验。 技术路线
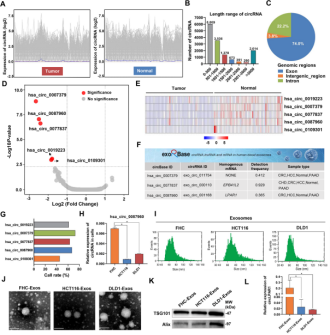
研究结果 一、下调的circLPAR1被包裹在结直肠癌的外泌体中 为了表征结直肠癌中失调的circRNA,作者在52对结直肠肿瘤和正常邻近组织(NAT)中进行了RNA-Seq,并观察到了14,221个circRNA。通过筛选,作者获得了5个circRNA(hsa_circ_0019223、hsa_circ_0007379、hsa_circ_0077837、hsa_circ_0087960和hsa_circ_0109301),与在NAT中的表达相比,它们在结直肠肿瘤组织中的表达显著降低。随后,作者使用exoRBase数据库对外泌体中的circRNA进行注释,并对来自NAT和结直肠癌的血浆外泌体以及结直肠癌细胞系进行circRNA的含量检测,最终发现hsa_circ_0087960(源自LPAR1,以下称为circLPAR1)在结直肠癌外泌体中表达,并在结直肠癌细胞系(HCT116和DLD1)中表达显著下调。
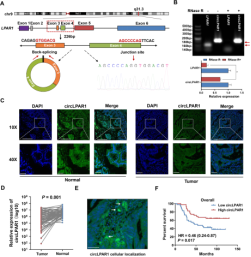
二、CircLPAR1在结直肠肿瘤中下调并与总生存期相关 CircLPAR1由位于chr9(113734352-113735838)上的LPAR1基因的外显子3和外显子4环化产生,长226bp,具有“头对尾”反向剪接位点。为了可视化circLPAR1的表达模式,作者使用包含79对结直肠肿瘤和NAT的组织微阵列进行了FISH测定,发现circLPAR1主要在细胞质中表达和定位。此外,当根据circLPAR1的中位表达对结直肠癌患者进行分层时,对数据的Kaplan-Meier分析表明,具有高circLPAR1水平的结直肠癌患者的总生存期明显优于那些患者。
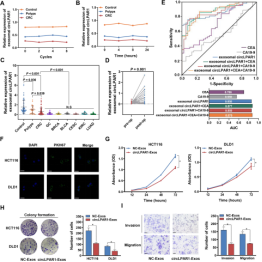
三、血浆外泌体circLPAR1是结直肠癌诊断的特异性生物标志物 考虑到外泌体中circLPAR1的检测及其在结直肠肿瘤中下调的表达模式,作者推测circLPAR1是否由血浆外泌体携带并可作为结直肠癌的特异性生物标志物。 作者对来自无癌对照、息肉患者、结直肠癌患者的外泌体circLPAR1进行了表达检测,发现结直肠癌外泌体显著低于无癌对照组和息肉患者,表明在从癌前病变到癌症的疾病发展过程中,外泌体circLPAR1可能会降低。此外,结直肠肿瘤切除后外泌体circLPAR1水平显著升高。ROC曲线显示,外泌体circLPAR1能够区分结直肠癌患者和无癌对照个体,并且AUC高于CEA和CA19-9(两种广泛用于结直肠癌诊断的临床生物标志物),外泌体circLPAR1、CEA和CA19-9的组合能够增加结直肠癌诊断的敏感性和特异性。 为了证明外泌体circLPAR1对结直肠癌细胞的作用,作者探索了外泌体circLPAR1在结直肠肿瘤发生中的生物学功能。作者将circLPAR1-Exos进行了荧光标记,荧光显微镜显示HCT116和DLD1细胞的细胞质中存在PKH67绿色荧光染料,而非Exos组中未观察到PKH67绿色荧光染料,表明HCT116/DLD1-Exos被结直肠癌细胞迅速吞噬。细胞功能实验表明外泌体circLPAR1显著抑制了结直肠癌细胞的增殖、集落形成、侵袭和迁移。
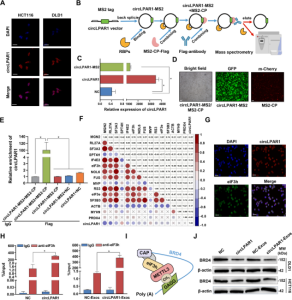
四、外泌体circLPAR1通过与eIF3h相互作用调节BRD4水平来抑制结直肠癌的肿瘤发生 为了探究外泌体circLPAR1影响结直肠癌的分子机制,作者进行了circRNApull-down和蛋白质组学检测,通过质谱分析和catRAPID发现eIF3h与circLPAR1的结合能力最强,并通过共定位实验和RIP-qPCR验证了外泌体circLPAR1直接与eIF3h相互作用。最近的一项研究报告称,eIF3h与甲基转移酶样3(METTL3)之间存在直接的物理和功能相互作用,可调节含溴结构域蛋白4(BRD4)的翻译并影响肿瘤发生。因此,作者想知道外泌体circLPAR1是否可以作为eIF3h的海绵来影响BRD4蛋白的表达。结果发现,与NC组相比,circLPAR1的存在降低了转染circLPAR1慢病毒载体或与circLPAR1-Exos孵育的结直肠癌细胞中的BRD4蛋白水平,暗示了外泌体circLPAR1能够通过与eIF3h相互作用来调节BRD4水平。
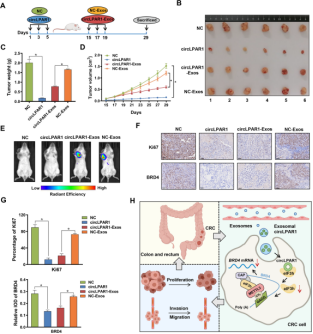
五、外泌体circLPAR1抑制体内结直肠癌生长 为了验证体内外泌体circLPAR1在结直肠癌中的抑制作用,作者将稳定的circLPAR1/NC过表达细胞注入人源化NCG小鼠,对小鼠的肿瘤表型、实时成像和IHC分析表明circLPAR1过表达或circLPAR1-Exos治疗降低了肿瘤的平均大小和重量。
结论: 在这项研究中,作者鉴定了一种新的circRNA,circLPAR1,它稳定地携带在血浆外泌体中,并成为一种潜在的结直肠癌特异性诊断生物标志物。机制上,外泌体circLPAR1被结直肠癌细胞内化并结合eIF3h以减少METTL3-eIF3h依赖的mRNA翻译,从而抑制BRD4表达并抑制细胞增殖、侵袭和迁移。该研究不仅报道了外泌体circRNA在结直肠癌中的新机制,而且为结直肠癌的筛查策略和诊断方法开辟了新途径。 |