NEWS
新闻资讯
|
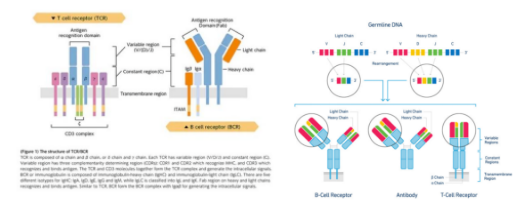
单细胞免疫组库在临床上的应用一、背景介绍 免疫系统是一个动态的综合网络,由分布在全身的不同细胞类型组成,它们共同作用以维持组织稳态并介导保护性免疫。不同的免疫细胞与异常细胞(如癌细胞)之间的相互作用,以及癌细胞对免疫细胞的响应与逃逸机制均不同,探究癌细胞-特定免疫细胞之间的作用机制有助于对癌症的精准免疫治疗。其中,T细胞和B细胞是适应性免疫应答的重要成分。 TCR(T cell receptor)是所有T细胞表面的特征标志,通常由α/β链组成,链上的高变互补决定区CDR3α和CDR3β环由可变(V)、多样性(D,仅β链)和连接(J)片段编码,并通过随机核苷酸插入进一步酶促多样化V-D-J基因片段的连接区域。CDR3α和CDR3β通过VDJ基因的重排,产生约1015到1020个独特的α和β对,随后与特定MHC分子-抗原肽复合物结合,完成对抗原的识别。与TCR类似,BCR(B cell receptor)是对应B细胞表面的特征标记,由重链和轻链组成,重链和轻链V(D)JC基因片段的“产生性重排”允许B细胞产生不同的BCR。一个成熟的T/B细胞只会产生一种特定的T/BCR,这种特性帮助我们抵御复杂多样的入侵分子。
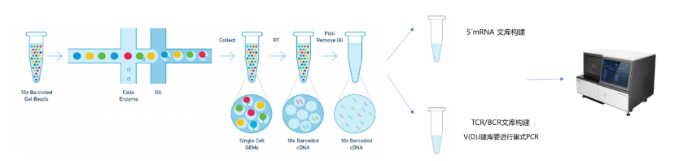
TCR/BCR结构图 为了分析TCR/BCR的作用机理,早期科学家使用多重PCR和5’RACE的方法进行样本中免疫组库的检测。然而这两个技术反映的是bulk级别样本中整体的免疫组库多样化的信息,并且具有一定的PCR偏好性或缺失。基于肿瘤/癌症的异质性,单细胞水平对癌症、免疫细胞的多样性与异质性研究正如火如荼,单细胞免疫组库也逐渐成为临床对免疫细胞研究的热点。 10X genomes平台的单细胞免疫组库(10X VDJ-seq)利用微流控、油滴包裹和barcode标记等技术来实现高通量的细胞捕获技术,能够一次性分离、并标记500–10000个单细胞,在单细胞水平同时检测转录组基因表达和TCR/BCR多样性,不但可以了解TCR/BCR克隆型,还可以联合转录组数据深入挖掘生命机理,为免疫组学研究提供更高效的平台,在肿瘤微环境、感染性疾病、自身免疫疾病等研究领域有着广泛的应用前景。
10X scVDJ-seq实验流程图 二、scVDJ-seq的应用 1、免疫微环境特征分析 研究多种疾病类型发生时免疫组库的变化,有助于揭示肿瘤的免疫微环境,从而辅助免疫治疗更好地抗击肿瘤。 文献案例: 一篇发表在Nature Medicine(IF=53.440)以COVID-19感染的肺泡灌洗液为研究对象,利用scRNA-seq和scTCR-seq描绘了与新冠肺炎COVID-19严重程度相关的免疫细胞特征,为理解COVID-19重症化免疫学机制提供了重要研究数据,为寻找疾病的免疫干预策略提供了重要线索。 文章标题: Single-cell landscape of bronchoalveolar immune cells in patients with COVID-19
摘要: 与2019冠状病毒病(COVID-19)严重程度相关的呼吸道免疫特征目前尚不清楚。通过单细胞RNA测序,作者对不同严重程度的COVID-19患者和健康人群的支气管肺泡灌洗液免疫细胞进行了特征分析。重症COVID-9患者支气管肺泡灌洗液中富含促炎单核细胞来源的巨噬细胞。中度病例的特点是存在高度克隆扩增的CD8+ T细胞。这张支气管肺泡免疫微环境图谱揭示了COVID-19发病和恢复的潜在机制。 2、药物治疗的免疫响应 药物治疗或免疫检查点(如PD-L1)治疗是目前对于癌症目前比较热门的医疗领域治疗方法,但并不是所有癌症或疾病都能够对其有良好的治疗响应。研究药物或免疫检查点治疗后免疫微环境的变化有利于揭示肿瘤的免疫逃逸机制。 文献案例: 一篇发表在Cancer Cell(IF=31.743)上的文章通过研究抗PD-L1和MAPK靶向治疗的顺序组合或单项治疗的单细胞免疫图谱,发现CD8+ T细胞和Ki-67hi T细胞以及对应的TCR克隆型与最有效疗法有明确关联性,揭示了组合治疗的免疫机制。 文章标题: Anti-PD-1/L1 lead-in before MAPK inhibitor combination maximizes antitumor immunity and efficacy
摘要: 合理测序并结合PD-1/L1和MAPK靶向治疗可能克服先天和后天耐药性。由于MAPK抑制剂(MAPKi)增加的临床效益与之前的免疫检查点治疗相关,作者比较了在BrafV600、Nras或Nf1突变驱动的黑色素瘤以及KrasG12C驱动的结直肠癌和胰腺癌的小鼠皮下模型中顺序和/或组合方案的疗效。抗PD-1/L1导入前MAPKi组合通过促进巨噬细胞的促炎极化和干扰素-γhi的克隆扩增,以及CD8+ T细胞毒性和增殖(相对于CD4+调节)T细胞高表达激活基因,从而优化反应持久性。由于黑色素瘤脑转移(MBM)的治疗耐药性限制了患者的生存,作者证明了MAPKi联合前的抗PD-1/L1治疗序列抑制了MBM,并通过在颅内和颅外转移部位的T细胞克隆扩增提高了小鼠的生存。作者建议在MAPKi联合治疗之前临床测试短暂的抗PD-1/L1(±抗CTLA-4)剂量以抑制治疗抵抗。 3、骨髓移植和免疫重建 器官或者骨髓移植时,经常会诱发宿主排斥反应的发生,从而发生慢性移植抗宿主病。此外,嵌合抗原受体T细胞(CAR-T)疗法由于显著的抗肿瘤作用,彻底改变了血液疾病恶性肿瘤的临床治疗。免疫组库测序技术可以检测移植后T细胞库,进行从而识别移植后感染或者复发的高危人群以及CAR-T治疗响应。 文献案例: 一篇发表在NC(IF=14.919)上的文章对接受CD19 CAR-T治疗的急性(复发性)淋巴细胞白血病患者中CAR-T细胞的克隆多样性变化,揭示了与输注后CAR-T细胞行为相关的转录程序。 文章标题: Clonal kinetics and single-cell transcriptional profiling of CAR-T cells in patients undergoing CD19 CAR-T immunotherapy
摘要: 嵌合抗原受体(CAR)T细胞治疗在B细胞恶性肿瘤患者中产生了显著的抗肿瘤反应。然而,调节CAR-T细胞输注后命运的克隆动力学和转录程序仍然知之甚少。在这里,作者通过TCRB测序、整合位点分析和单细胞RNA测序(scRNA-seq)来分析来自输液产品(IPs)和接受CD19 CAR-T免疫治疗患者血液中的CD8+ CAR-T细胞。TCRB测序显示,CAR-T细胞的克隆多样性在IP中最高,并且在输注后下降。作者观察到表现出不同克隆动力学模式的克隆,在输注后对CAR-T细胞池做出了不同的贡献。虽然整合位点似乎不是克隆动力学的关键驱动因素,但scRNA-seq表明,输注后扩增的克隆主要来自具有较高细胞毒性和增殖基因表达的输注簇。因此,作者揭示了输注后与CAR-T细胞行为相关的转录程序。 4、新靶点的开发 药物靶点是指药物在人体内的作用结合位点,不同的疾病/组织类型对相同的药物响应是不一样的,多位点药物靶点的寻找有利于后续临床开发靶向这些靶点的免疫治疗药物,从而能够使得更多患者对治疗产生正向反应。 文献案例: 一篇发表在Sci Immunol(IF=17.727)上的文章探究了肿瘤引流区淋巴结(dLN)中的干细胞样(Stem-like)CD8+ T细胞在肿瘤进展过程中的维持机制。为对PD-1阻断治疗反应较差的免疫“冷”肿瘤(非T细胞炎症)患者的预后提供了基于识别针对dLN中肿瘤特异性T细胞的新治疗策略。 文章标题: A reservoir of stem-like CD8+ T cells in the tumor-draining lymph node preserves the ongoing antitumor immune response
摘要: 肿瘤中“干细胞样”TCF1+CD8+T(TSL)细胞的存在与免疫治疗后更好的患者预后相关。TSL细胞在肿瘤微环境中经历终末分化和衰竭;因此,在整个肿瘤发展过程中如何维持干细胞样种群尚不清楚。Connolly等人使用编程为表达新抗原的肺腺癌小鼠模型,在肿瘤引流淋巴结(dLN)中发现了一个稳定的肿瘤特异性TSL细胞库。随着肿瘤微环境从“热”转变为“冷”,TSL细胞从dLN迁移到肿瘤并最终分化。这些发现表明,针对dLN中肿瘤特异性T细胞的治疗策略可能是治疗冷肿瘤患者的一种有前途的方法。 三、总结与展望 ScVDJ-seq的可行性推动了T/B细胞领域的快速发展,首先,它帮助揭示了临床疾病的免疫图谱以及免疫响应,同时,一些新靶点的发现还有利于靶向药物的开发。然而,这项技术目前仍然具有一定的局限性,例如细胞的捕获效率可能限制一些罕见亚群的发现与分析,单细胞测序的成本仍较高等等。另外,由于针对于人和小鼠的VDJ区域研究较多,成熟的VDJ富集产品目前仅限于人和小鼠,对于一些研究非模式生物的老师限制会更大。期望在不久的将来,对这些挑战能有更好的改进工作,从而适配更多老师的研究需求! |