NEWS
新闻资讯
|
客户文章 | IF=15.328!单细胞测序揭示胶质母细胞瘤中恶性细胞与血管细胞的谱系关系
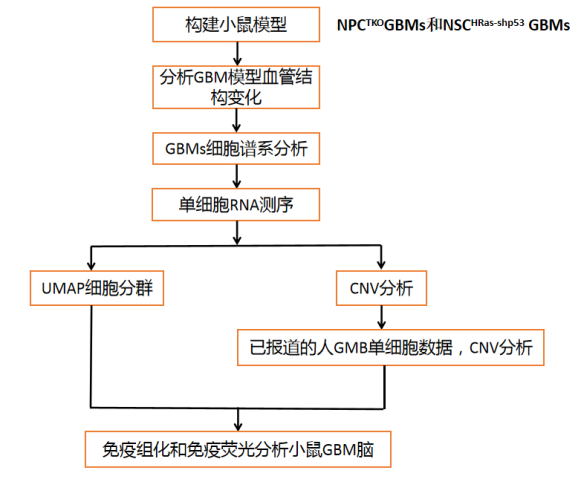
发表单位:武汉大学中南医院 发表日期:2022年5月18日 期 刊:Protein & Cell(IF:15.328) 2022年5月18日,武汉大学中南医院神经外科在期刊Protein & Cell(IF:15.328)发表题为“Resolving the lineage relationship between malignant cells and vascular cells in aglioblastomas”的研究论文。该研究在小鼠中生成了2个遗传GBM(Glioblastoma multiforme,胶质母细胞瘤)模型,模拟人类GBM的基础病理和分子特征。作者对谱系进行了追踪,并利用单细胞RNA-seq对拷贝数变异进行了分析。该研究促进了对GBM细胞谱系潜力的理解,并可能为GBM患者的靶向治疗提供见解。爱基百客为该研究提供单细胞测序和分析的技术支持。
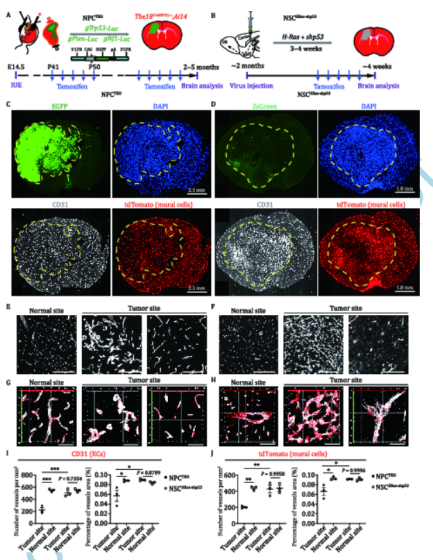
研究背景 多形胶质母细胞瘤(Glioblastoma multiform, GBM)是一种高度恶性、异质性的脑肿瘤,包含多种类型的肿瘤和非肿瘤细胞。GBM细胞是否可以转分化为非神经细胞类型,包括壁细胞或内皮细胞,以支持肿瘤生长和侵袭仍存在争议。破译GBM微环境的细胞组成和谱系历史,包括内皮细胞、壁细胞和肿瘤相关的小胶质细胞和巨噬细胞,对开发GBM的靶向治疗具有重要意义。GBM细胞被认为起源于突变的神经干细胞/祖细胞。先前的研究表明,GBM干细胞可能产生血管内皮细胞(ECs)或壁细胞支持肿瘤生长和侵袭。作者早期的研究还发现,干细胞标志物既可以标记胶质瘤干细胞样细胞,也可以标记壁细胞,提示胶质母细胞瘤细胞可能存在跨谱系的转分化。 最新的单细胞技术结合谱系追踪分析,对理解在发育过程、组织稳态、再生和病理条件下的细胞成分、细胞状态和命运分化有深刻的意义。 研究思路 研究结果 1. 建立遗传GBM模型以追踪GBM细胞的命运 构建NPCTKOGBMs小鼠模型。作者首先利用遗传小鼠GBM模型来研究胶质瘤细胞是否可以产生非神经细胞。通过失活Trp53、Pten和Nf1将胚胎神经祖细胞(NPCs)转化为GBM起始细胞(GICs),它们是人类GBM中突变最多的三种肿瘤抑制因子。这种GBM模型被命名为NPCTKO。利用Cas9基因编辑技术与谱系标记,通过荧光素介导的成像分析筛选成年小鼠的脑肿瘤。根据所使用的谱系标记的不同,肿瘤肿块广泛用胞质EGFP或DsRed标记。 对GBM切片染色,分别有神经元细胞(NeuN)、少突细胞(MBP)、星形胶质细胞(GFAP)、人少突胶质细胞前体细胞(OPC,OLIG2)和神经干细胞(SOX2)的标记。大约有50-80%的GBM细胞表达OLIG2,10%表达GFAP,暗示大部分的GBM细胞的OPC特征与OPC样GBMs中观察到的细胞特性一致。此外,大约60%-80%的肿瘤细胞也表达SOX2,表明其未分化状态。 构建NSCHRas-shp53 GBMs小鼠模型。作者通过将成年神经前体原位转化为GBM起始细胞,建立了另一个GBM遗传模型(图1B)。共表达Trp53 shRNAs和人组成型激活的HRASG12V致癌基因的慢病毒注射进成年C57BL/6小鼠(NSCHRas-shp53)的脑室-室下区,在注射病毒后的3-4周发展成具有典型GBM组织病理学特征的高级别胶质瘤。小鼠NSCHRas-shp53 GBMs的单细胞RNA-seq分析显示在人类GBM中鉴定发现每个肿瘤包含3个细胞状态,包括OPC样、星形胶质样和MES样。NSCHRas-shp53 GBMs比NPCTKOGBMs包含更少的OLIG2表达细胞。转录组分析暗示3个NSCHRas-shp53 GBMs分子上再现了人类GBMs的TCGA-MES亚型。 2. GBM肿瘤发生诱导广泛的脑血管改变 作者随后研究了这两种类型的GBMs如何影响大脑中的血管结构。在Tbx18CreERT2/+;Ai14脑中重新生成NPCTKO和NSCHRas-shp53GBMs,其中壁细胞在他莫西芬的作用下被遗传标记。在两种模式下,ECs(内皮细胞)的CD31信号增强,许多肿瘤血管得到扩张、变硬、集中或高度散乱(图1C-H)。令作者惊讶的是,在NPCTKO型GBMs中,相对于非肿瘤位置,肿瘤区域的血管较少,且血管覆盖减少,血管表现为肾小球样。与NPCTKO型GBMs相比,NSCHRas-shp53型GBMs中血管大幅扩张并交织成网状结构,血管密度和血管面积增加(图1E-J)。由于NPCTKO GBMs比NSCHRas-shp53 GBMs含有明显更多的OLIG2+细胞,这些观察结果与先前的研究一致,显示OLIG2阳性的GBMs具有几乎正常的血管,而OLIG2阴性的GBMs促进血管生成和血脑屏障(BBB)破坏。
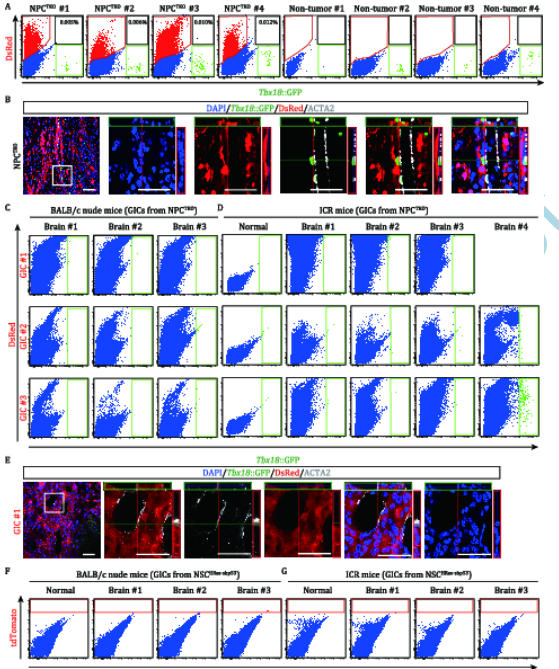
图1 脑胶质瘤形成引起广泛的脑血管改变 3. GBM细胞向壁细胞的最小转分化 接下来,作者探索了GBM细胞向壁细胞转分化的可能性。转染怀孕的Tbx18H2B-GFP/+小鼠让作者可以检查NPCTKO GBMs中DsRed标记的恶性细胞的命运选择。流式细胞术分析显示,DsRed+GBM细胞与Tbx18::H2B-GFP+壁细胞为独立群体,仅有极少数双标记细胞(图2A),后者可能是一些GBM细胞少见的转分化事件或错误表达Tbx18。 肿瘤切片用Tbx18::H2B-GFP和平滑肌肌动蛋白α2(ACTA2)进行免疫组化染色,共聚焦成像和三维重建显示,虽然许多DsRed+ GBM细胞靠近血管,但未检测到GBM细胞与ACTA2信号或Tbx18::H2B-GFP重叠。
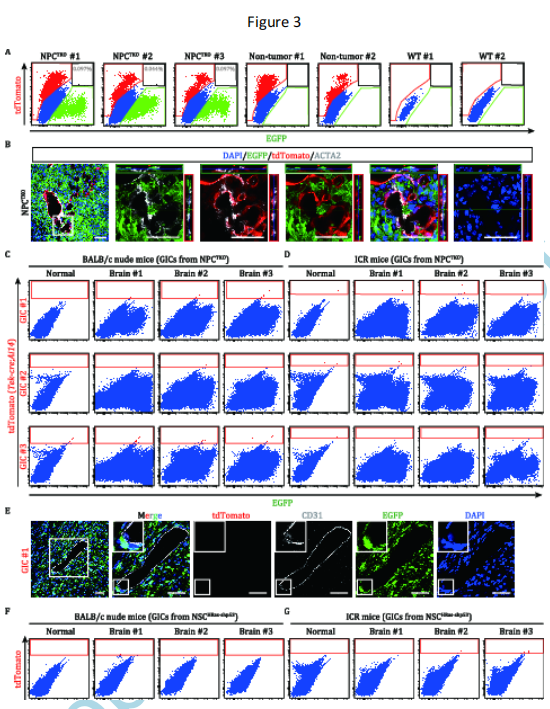
图2 恶性胶质瘤细胞在GBM脑中很少产生壁细胞,但可在异体移植时混杂表达Tbx18 4. 颅内移植后GBM干细胞样细胞分化为壁细胞的可能性很小 作者将DsRed+ GICs移植到裸小鼠和ICR小鼠的颅内以产生同种异体移植肿瘤。颅内肿瘤切片IF染色未见DsRed+/Tbx18::H2B-GFP+或DsRed+/ACTA2+双阳性细胞(图2E)。通过流式细胞术,虽然9例裸脑移植或11例ICR移植中均没有检测到Tbx18::H2B-GFP+双阳性细胞,两例ICR移植物中含有非常小比例的Tbx18::H2B-GFP细胞:在分析的280万个细胞中,两个ICR移植物中分别只检测到365和3523个Tbx18::H2B-GFP细胞(图2C和D)。然而,这些Tbx18::H2B-GFP细胞不表达ACTA2,并且远离ACTA2标记的血管。另外,作者还将GICs移植到裸小鼠和ICR小鼠里进行观察。这部分分析结果证明GICs在异体移植或异种移植的动物中几乎不能分化为壁细胞,尽管在胶质瘤形成过程中很少有一小部分GBM细胞表达壁细胞标记物。 5. GBM细胞不能向内皮细胞转化 为了探讨GBM细胞向造血或内皮系转分化的可能性,作者在Tek-Cre;Ai14脑中生成的NPCTKO和NSCHRas-shp53GBMs进行谱系追踪研究。与图2A中显示的结果类似,Tek- Cre标记的EGFP+ GBM细胞和tdTomato+细胞是不同的群体,只检测到一小部分双标记细胞(图3A),可能是由于在肿瘤发生过程中少数GBM细胞误表达Tek所致。许多肿瘤血管被表达acta2的壁细胞完全或部分覆盖(图3B)。
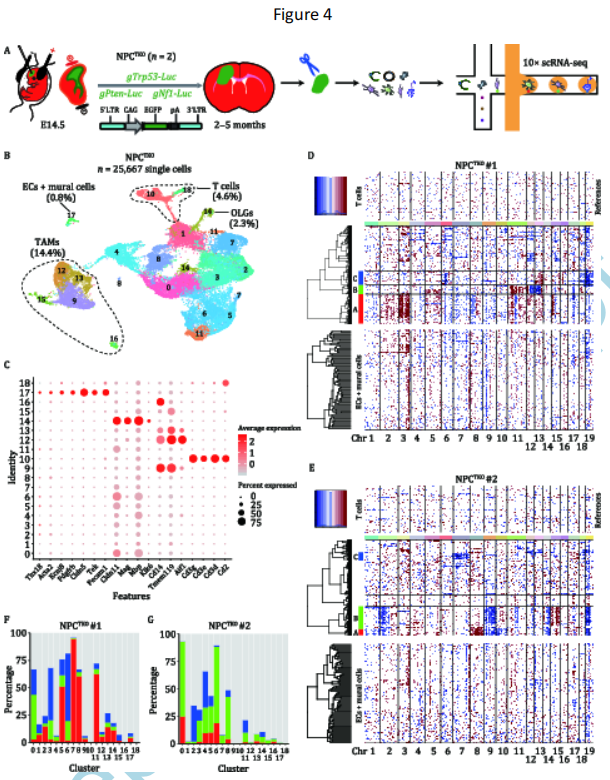
图3 在遗传性胶质母细胞瘤大脑中,胶质母细胞瘤细胞不产生内皮细胞(ECs)和肿瘤相关的小胶质/巨噬细胞(TAMs) 6. GBM干细胞样细胞颅内移植后EC分化的缺失 接下来,将来自3个Tek-Cre;Ai14 GBMs的EGFP+ GICs移植到免疫受损的BALB/c裸鼠或免疫正常的ICR小鼠的大脑中,产生同种异体移植瘤。在流式细胞实验中,没有检测到来自移植肿瘤的EGFP+/tdTomato+细胞(图3C和D)。 为了探究来自NSCHRas-shp53肿瘤的GBM细胞是否能产生ECs,作者还将NSCHRas-shp53 (Tek-Cre;Ai14) GBMs富集的GICs植入BALB/c裸鼠和ICR小鼠的大脑中。与使用NPCTKO GICs的发现一致,通过流式细胞术,没有检测到来自NSCHRasshp53 GICs移植肿瘤的tdTomato+细胞(图3F和G)。在作者设置的实验中,无论在免疫受损或免疫正常条件下,GICs都不会在体内产生ECs。 7. GBM细胞的单细胞RNA测序将肿瘤与非肿瘤细胞类型区分开来 接下来,作者利用单细胞RNA测序(scRNA-seq)来表征GBM样本中不同的细胞类型,然后分析恶性细胞和血管细胞之间的谱系关系。然后将已建立的标记基因映射到UMAP代表指定细胞类型。来自NPCTKO模式的2个GBM样本(要么来自Tek-Cre;Ai14要么来自Tbx18CreERT2/+;Ai14 脑),解剖然后酶解成单细胞悬液,然后提交到10XGenomics scRNA-seq试验系统中。共有25667个单细胞成功测序(图4A)。 使用UMAP对细胞群降维,细胞群分为18个主要的细胞簇(图4B)。将已完善的标记基因映射到UMAP上来代表指定的细胞类型。血管细胞(Pecam1、Cldn5和TeK对应内皮细胞;Pdgfrb、Kcnj8、Acta2和Tbx18对应于壁细胞)、肿瘤相关小胶质细胞/巨噬细胞(Cd14、Aif1和Tmem119)、少突细胞(Klk6、Mag、Mbp和Cldn11)和T淋巴细胞(Cd2、Cd3d、Cd3e和Cd3g)分别聚集到不同组。值得注意的是,集群的内皮细胞与壁细胞要么不可分离,要么相互接近,表明它们有亲缘关系。 假定的肿瘤细胞(图4B-C)广泛表达神经干细胞标记基因(Sox2、Nestin和Olig2)和Pdpn(GBM细胞间充质样状态的标志)。正如预期,荧光素酶和Egfp在具有NSC特征的细胞中检测到表达最多。然而,内皮细胞或壁细胞的标记物的表达并不局限于维管束细胞,但也可以在其他细胞类型中检测到,尽管水平相对较低。这个对Cspg4(Ng2)尤为正确,是一个标记OPCs的标记,在GBM细胞中高表达。尽管tdTomato主要在维管束细胞和TAMs中表达,在其他细胞群中也能检测到,表明在GBM肿瘤发生过程中血管细胞标志物的异常表达。另一方面,NSC的标记物表达也能在非神经细胞中检测到相对温和的表达水平,这与近期的关于人类GBMs的scRNA-seq研究相呼应(Bhaduri et al., 2020)。 此外,相当一部分肿瘤细胞和非肿瘤细胞表达Mki67,提示其增殖状态。总之,对NPCTKO型胶质母细胞的scRNA-seq数据的分析支持了作者的谱系追踪分析,表明尽管血管细胞和TAMs聚集在明显不同于恶性细胞的组中,一些GBM细胞混杂地表达其他谱系的标志物,因此在分配细胞类型之前需要极其谨慎通过使用一些单独的标记来鉴定。
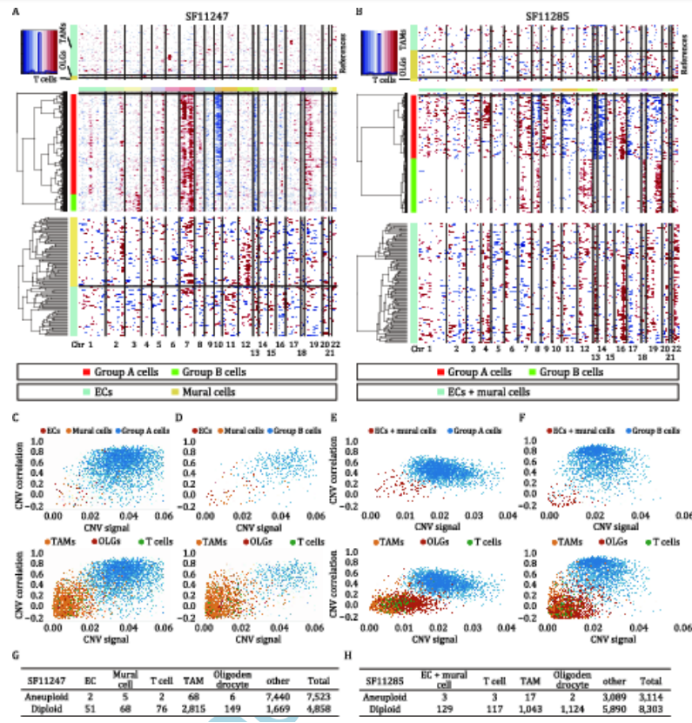
图4 NPCTKOGBM样本中血管细胞和恶性细胞的CNV模式及分布 8. 血管细胞的拷贝数变异与GBM细胞的不同 具有共同祖先的细胞具有类似的遗传变异,如拷贝数变异(CNV),最近的研究根据CNVs分析了谱系关系。为了进一步探索肿瘤细胞和非肿瘤细胞之间的谱系关系,作者利用scRNA-seq数据比较了GBM细胞和血管细胞的CNV特征。作者推测如果ECs和壁细胞是由GBM细胞转分化而来,它们应该与肿瘤细胞共享相同的CNVs。 于是利用T细胞的CNV作为参考,对NPCTKO GBM样本进行了CNV分析(如4D-E)。采取inferCNV算法,通过对分析基因的染色体位置进行排序来估计CNVs,对相对表达值应用移动平均,每条染色体内有100个基因的滑动窗口。分层聚类将剩余的单个细胞根据其CNV特性分组为多个细胞组。CNV分析发现基于它们主要的CNV特征在两个NPCTKO GBM样本中鉴定到3组恶性细胞(组A/B/C),包括基因组缺失和扩增,显示肿瘤内和肿瘤间异质性。作者发现血管细胞和恶性细胞的CNV模式不同。根据转录组特征识别为恶性细胞的被分配到以往报道过的细胞群中(图4B和C)。2个NPCTKO GBMs的0、3、4、5、6、7、8和11簇中含有大量恶性细胞。来自2个NPCTKO GBMs样本的超过90%的血管细胞被指定为良性细胞(图4F和G)。对于少数成簇分到血管细胞的恶性细胞,作者推断这些细胞可能表现出一些血管细胞的转录组特征。此前有报道显示部分血管细胞可通过克隆扩张获得恶性细胞的某些CNV特性。 接下来,作者将CNV信号以及血管细胞和T细胞之间的相关性叠加在每批恶性细胞上。“CNV信号”反映了每个细胞CNV的总体程度,定义为整个基因组中CNV值的平方的平均值。在2个NPCTKO GBM样本的3个恶性细胞簇中,血管细胞和T细胞的CNV特性与恶性细胞很大程度上不同,这一结果支持这些细胞类型的不同谱系起源。值得注意的是,NSCHRas-shp53 GBM细胞的拷贝数变异没有NPCTKO GBM细胞激烈,这可能是由于不同的癌驱动因子和/或NSCHRas-shp53 GBM胶质瘤形成期较短。 9. 在人类GBM样本中,血管细胞的CNVs与恶性细胞不同 为了研究人类GBM的上皮细胞和壁细胞来自恶性细胞的可能性,作者分析了人类GBM样本的CNV特征。选取了来自Bhaduri et al研究2个人GBM样本(SF11247和SF11285)的scRNA-seq数据进行分析。SF11247样本有12398个细胞分为18个簇,内皮细胞和壁细胞在距离近但不同的簇中。SF11285样本有11433个细胞分为14个簇,内皮细胞和壁细胞在同样的簇中。与小鼠GBM样本的结果相似,大多数血管细胞标志物的表达也可以在其他细胞类型中检测到。 利用scRNA-seq数据进行CNV分析,以T细胞、TAMs和少突胶质细胞的CNV为参考。作者根据其CNV特性将每个样本的GBM细胞分为两组(图5A和B)。SF11247的A组细胞表现出GBM的特征——7号染色体重复和10号染色体缺失;而B组细胞表现出3号和10号染色重复,以及13号染色体缺失(图5A)。至于样本SF11285,A组细胞存在广泛的扩增和缺失;但B组细胞在7、8、12、18和19号染色体上存在显著的扩增(图5B)。与小鼠遗传模型获得的数据一致,血管细胞的CNV模式明显不同于肿瘤细胞。尽管一些血管细胞与恶性细胞有一些共同的CNV特征,包括16号染色体扩增,但血管细胞有特有的拷贝数变异,如13号染色体扩增在SF11285中监测到(图5B),这表明在染色体异常之后可能会出现克隆扩增。这与最近的一份报告发现的结果相似,该报告发现人类结直肠癌的一些基质细胞,包括免疫细胞、成纤维细胞和内皮细胞,可能由于克隆扩张而产生具有不同特征的基因组改变。 然后,作者计算并比较了CNV信号和CNV与恶性细胞的相关性。在两个肿瘤中,与非肿瘤TAMs、少突胶质细胞和T细胞类似,大多数血管细胞CNV信号较低,与GBM细胞相关性较低(图5C-F),形成不同的群体。因此,在小鼠和人类GBM中,血管细胞的CNV特性与恶性细胞不同,这强烈表明血管细胞来源于GBM细胞以外的细胞系。值得注意的是,小比例的T细胞、TAM和少突胶质细胞也被划分为非整倍体细胞(图5G和H)。
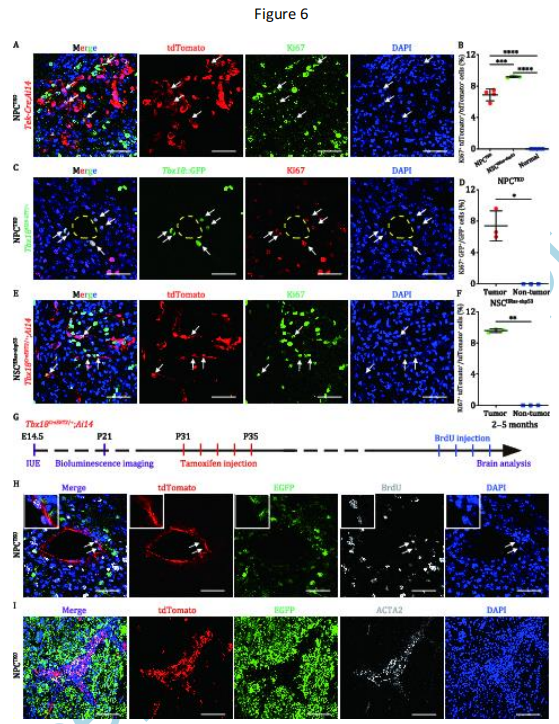
图5 人GBM细胞和血管细胞的CNV模式是分开的 10. 内皮细胞和壁细胞在GBM发生过程中增殖 为了进一步研究增殖的细胞类型,NPCTKO和NSCHRas-shp53脑肿瘤切片用Ki67共免疫组化染色。结果表明,在NPCTKO GBM脑中,Tek-Cre;Ai14小鼠tdTomato+细胞中约7%为Ki67+增殖细胞,Tbx18::H2BGFP+细胞中约7%为Ki67+增殖细胞,而对侧相应脑区无标记+/Ki67+细胞(图6 A-D)。在Tek-Cre;Ai14小鼠和Tbx18::H2BGFP+小鼠中NSCHRas-shp53GBM脑中包含约9%的tdTomato+Ki67+细胞(图6B、6E和6F)。 取2-5个月大小鼠的脑瘤进行免疫荧光分析,在实验前给小鼠连续4天喂BrdU(图6G)。结果表明,NPCTKO GBM脑遗传标记的ECs和壁细胞约10%已包含了BrdU(图6H)。最后,GBM小鼠脑中的所有ACTA2+壁细胞是NPCTKOGBM脑中Tbx18-CreERT2;Ai14细胞的后代(图6I)。总之,研究结果表明GBM组织中主要血管细胞类型的扩增是自繁殖的结果,而不是通过GBM细胞转分化产生的。
图6 在胶质瘤形成过程中,内皮细胞和壁细胞自我增殖 总结在该研究中,通过仔细的谱系追踪和单细胞分析,没有观察到GBM细胞向血管细胞的跨谱系转分化。然而,考虑到GBM在肿瘤间和肿瘤内的高度异质性,作者不能排除少数GBM细胞可能获得血管细胞的一些分子和功能特征。谱系追踪研究确实显示,一小部分GBM细胞错误表达了血管细胞的标记物;少数NPCTKO GBM血管细胞根据其CNV特性被确定为恶性细胞。因此,用单细胞测序补充遗传谱系追踪实验可以更严格地识别谱系关系。未来的研究应更多地应用其他壁细胞或内皮细胞标记物进行谱系追踪研究。此外,单细胞测序和CNV分析,然后使用附加的GBM样本富集血管细胞,可以进一步提高分化谱系的分辨率。总之,该研究的发现促进了对GBM细胞谱系潜力的理解,并可能为GBM患者的靶向治疗提供见解。 文献资料 文献下载
|