NEWS
新闻资讯
|
客户文章 | IF=23.168!CLK1-SRSF5轴在胰腺癌中的作用机制及预后价值
发表单位:福建医科大学和瑞金医院 发表日期:2021年4月13日 期 刊:J Hematol Oncol(IF: 23.168) 2021年4月13日,福建医科大学和瑞金医院研究团队在著名期刊Journal of Hematology & Oncology(IF: 23.168)发表题为“CLK1/SRSF5 pathway induces aberrant exon skipping of METTL14 and Cyclin L2 and promotes growth and metastasis of pancreatic cancer”的研究论文。该研究首次系统地评估了CLK1-SRSF5轴在胰腺癌发生发展中的作用,以及该通路的预后价值。爱基百客为该研究提供了CLIP-qPCR技术支持。
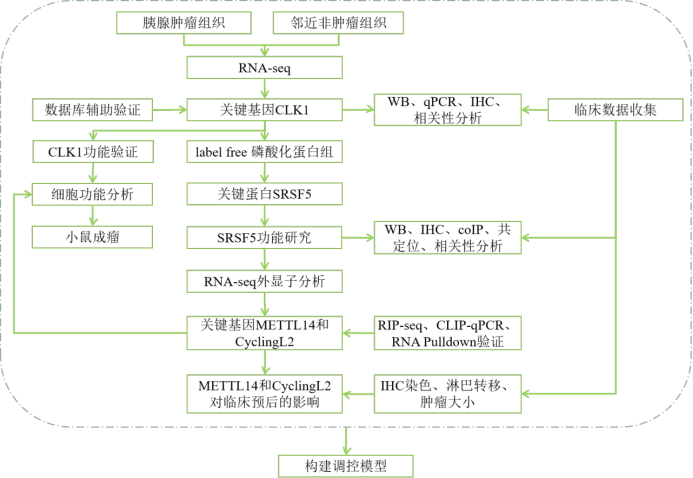
一、研究背景 作为世界上第四大癌症相关死亡原因,胰腺癌(PC)通常在晚期被诊断出来。迄今为止,PC的五年生存率仅为8%,大多数患者在手术后7年内死亡,表明PC患者的预后非常差。尽管对PC的累积遗传研究已经确定了关键基因的大量改变,PC发展背后的分子机制还有很多待发现。因此,迫切需要寻找有效的治疗策略,以促进早期发现并改善PC的预后,例如常见的胰腺导管腺癌(PDAC)。 作为最普遍的基因调控机制,选择性剪接(AS)和N6-甲基腺苷(m6A)已成为人类癌症中普遍存在的基因修饰,剪接因子已被证实是多种恶性肿瘤的致癌或抑制驱动因素。此外,异常m6A修饰与肿瘤发生和肿瘤发展有关,在此过程中,“Writer”METTL14的蛋白质效应是显著的。然而,目前为止包括METTL14在内的m6A修饰相关蛋白的选择性剪接功能在国际上尚未见报道。因此,探索METTL14剪接介导的m6ARNA甲基化在肿瘤发生和癌症发展中可能很有趣。 富含丝氨酸/精氨酸的剪接因子(SR)属于RNA结合蛋白(RBP)的剪接因子类别,可调节RNA剪接和其他RNA修饰相关事件,磷酸化对于SR蛋白的剪接和剪接独立功能都至关重要,由经典SR剪接因子(SRSF)和RNA结合SR样剪接因子组成。据报道,SRSF5在多种癌症中异常表达,然而,SRSF5在胰腺癌中的功能尚未得到深入阐明。 为此,本文进行了多组学分析,旨在寻找胰腺癌中选择性剪接与m6A甲基化之间的关系,为开发针对胰腺癌患者的有效疗法提供新思路。 二、文章思路
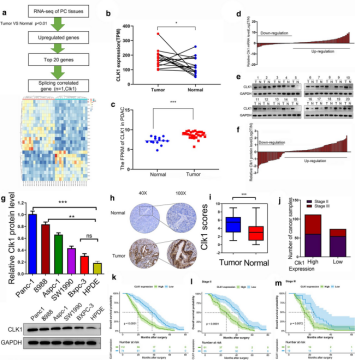
三、研究材料 (1)15对PDAC和胰腺正常组织;——RNA-seq、WB (2)102对PDAC和胰腺正常组织;——qPCR (3)正常人胰管上皮细胞和不同的人胰腺癌细胞系(三组生物学重复);——WB、coIP、label free磷酸化蛋白组、细胞功能分析、小鼠成瘤实验、RNA-seq(AS分析) (4)186例胰腺癌患者石蜡包埋样本;——IHC (5)344名患者;——临床表型 四、研究结果 4.1胰腺癌组织中CLK1表达升高与PDAC患者预后恶化相关在由15对配对的PDAC和胰腺正常组织组成的样本中进行高通量测序。CLK1被鉴定为唯一一个与剪接相关的过表达基因,并被选择用于后续实验。公共数据库GEO和TCGA数据库的数据也证实CLK1在大多数胰腺癌组织中比正常组织表达量高。此外,与正常人胰管上皮(HPDE)细胞相比,包括PANC-1、8988、Aspc-1、SW1990、BxPC-3在内的人胰腺癌细胞系的CLK1表达更高。IHC结果、临床病理特征也表明CLK1的表达升高与PDAC患者的预后较差相关。
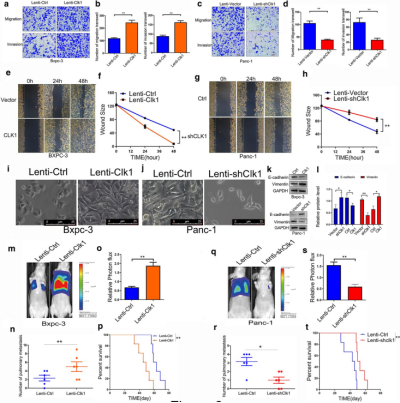
图1胰腺癌组织中CLK1表达升高与PDAC患者预后恶化相关 4.2 CLK1在体外和体内促进人胰腺癌细胞的生长为了检测CLK1表达对胰腺癌生长的影响,作者构建了CLK1过表达和敲低细胞系,进行了细胞增殖、迁移功能分析以及小鼠成瘤实验,发现CLK1能够通过在体内和体外促进胰腺癌细胞的增殖和迁移而起到致癌因子的作用。
图2 CLK1可增强人胰腺癌细胞的体内外增殖能力
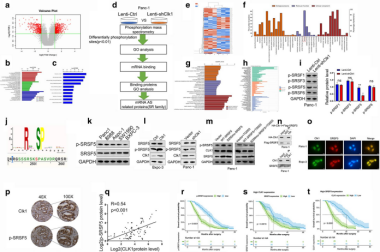
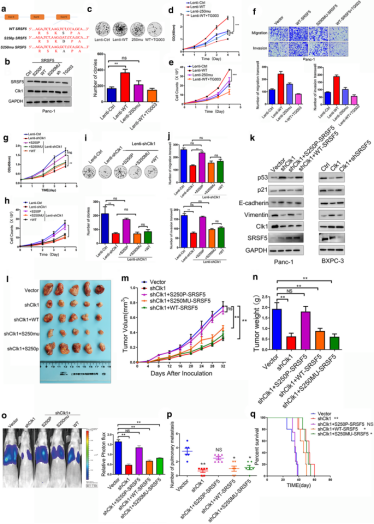
图3 CLK1促进胰腺细胞在体内外的迁移和侵袭能力 4.3 CLK1广泛参与选择性剪接相关蛋白的磷酸化调控,尤其是SRSF5-ser-250由于CLK1是一种磷酸化激酶和选择性剪接因子,作者进行了label free磷酸化质谱分析来探索CLK1的目标磷酸化蛋白。结果发现CLK1广泛参与选择性剪接相关蛋白的磷酸化调控,其中SRSF5-ser-250位点可能是CLK1潜在的重要靶点(通过WB、IHC、coIP实验进行了验证)。为了探索SRSF5对Ser-250磷酸化在调节PDAC细胞恶性行为中的作用,作者构建了SRSF5突变系、模拟磷酸化ser位点系,并结合野生型CLK1和CLK1过表达进行了细胞增殖、迁移分析和小鼠成瘤实验。发现SRSF5-Ser-250磷酸化能够促进胰腺癌细胞的增殖和迁移,并促进肿瘤生长。表明CLK1介导的SRSF5在Ser-250上的磷酸化是CLK1在胰腺癌中的促癌功能的潜在机制。
图4 CLK1可磷酸化人胰腺癌细胞中的SRSF5-ser-250
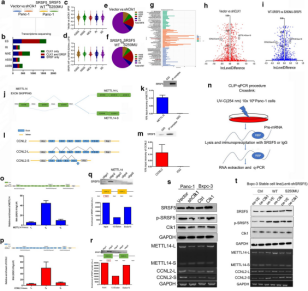
图5 CLK1诱导的SRSF5-Ser-250磷酸化有助于胰腺癌细胞的增殖和转移 4.4 SRSF5控制胰腺癌细胞中METTL14和CyclinL2的外显子跳跃为了全面了解由CLK1介导的Ser-250上的SRSF5磷酸化调节的选择性剪接事件,作者对CLK1对照组和CLK1过表达组进行了RNA-seq,通过对可变剪接分析,发现了METTL14和CyclinL2的可变剪切事件。随后,RIP-seq分析、CLIP-qPCR和RNA Pulldown实验结果表明,CLK1对Ser-250上的SRSF5的磷酸化促进了SRSF5与METTL14和CyclinL2的前体mRNA之间的相互作用以及随后的外显子跳跃调节。
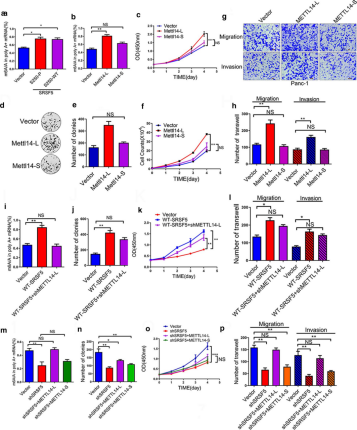
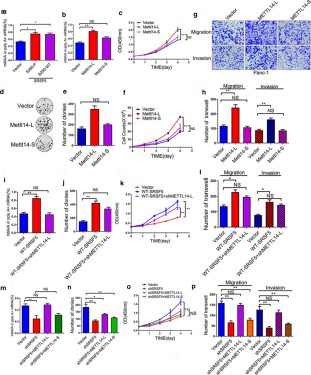
图6 SRSF5控制METTL14和CyclinL2的外显子跳跃 4.5 CLK1-SRSF5通过调控METTL14和CyclinL2的外显子跳跃来调控细胞增殖考虑到METTL14主要参与调节m6A,作者分析了METTL14可变剪接对m6A水平的影响。作者构建了CLK1过表达、SRSF5磷酸化过表达、METTL14-L过表达等体系并检查了m6A水平、细胞增殖和转移水平,发现SRSF5能够通过抑制METTL14的外显子跳跃来提高m6A水平并促进细胞增殖和迁移。 据报道,CyclinL2在许多类型的癌症中调节细胞周期和增殖,作者构建了CyclinL2外显子跳跃和对照组,通过细胞增殖和迁移试验发现CyclinL2的外显子跳跃能够促进细胞增殖,而这种跳跃是受SRSF5调控的。 为了进一步阐明METTL14/CyclinL2的可变剪接与胰腺癌患者临床预后的关系,作者对临床样本中P-SRSF5的表达与METTL14和CyclinL2的PSI偏移的关系进行了评估,发现若METTL14和CyclinL2发生异常选择性剪接,能够对PDAC患者产生潜在的预后价值。 作者首次系统地评估了CLK1-SRSF5轴在胰腺癌发生发展中的作用,以及该通路的预后价值。在机制上,作者证明CLK1-SRSF5轴通过促进CyclinL2△exon 6.3跳跃促进胰腺癌增殖,并通过抑制METTL14△exon 10跳跃增强细胞迁移和侵袭的能力。基于评估结果,作者最后构建了一个CLK1-SRSF5轴的工作模型。
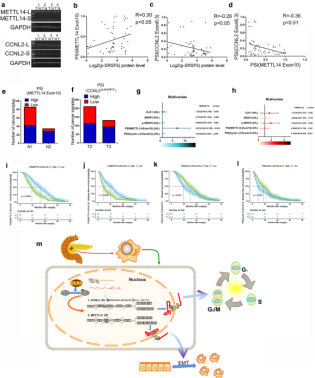
图7 SRSF5通过抑制METTL14△exon 10跳跃性,提高PC细胞m6A水平,促进细胞增殖和转移
图8 SRSF5通过促进cyclinL2△exon6.3跳跃性,促进PC细胞肿瘤的增殖
图9 METTL14△exon 10和CyclinL2△exon 6.3的异常选择性剪接对PDAC患者具有预后价值 五、文章结论 作者首次系统地评估了CLK1-SRSF5轴在胰腺癌发生发展中的作用,以及该通路的预后价值。在机制上,作者证明CLK1-SRSF5轴通过促进CyclinL2△exon 6.3跳跃促进胰腺癌增殖,并通过抑制METTL14△exon 10跳跃增强细胞迁移和侵袭的能力。值得注意的是,作者是第一个通过影响METTL14△exon10的可变剪接模式来证明CLK1-SRSF5轴在调节胰腺癌中m6A甲基化中的关键作用。该研究为靶向CLK1-SRSF5轴和m6A调节因子以开发针对胰腺癌患者的有效疗法提供了新思路。 往期推荐: 文献下载
|