NEWS
新闻资讯
|
一文get国自然热点“组蛋白乳酸化”的研究方向和思路作为近些年的国自然热点,“组蛋白修饰”不仅是细胞记忆的守护者,也是生命过程调控的重要的参与者。组蛋白是构成染色质的基本蛋白质单位,它们能够通过各种化学修饰如乙酰化、甲基化、磷酸化和乳酸化等,精确调控基因的表达,影响细胞的命运决策。 作为调控基因表达和细胞命运的重要手段,组蛋白修饰不仅是细胞内部信息传递的重要环节,也是连接遗传信息和环境因素的桥梁。其中,2019年首次发现的组蛋白乳酸化因其与糖酵解的关系,逐渐成为科研热点,备受基金项目和期刊的亲睐。近三年,相比其他组蛋白修饰,国自然中标基金中,组蛋白乳酸化已逐渐成为最热门的修饰之一。
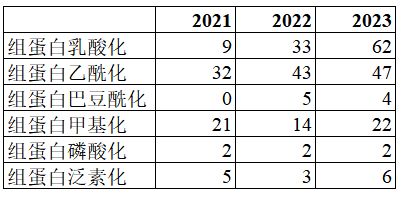
部分组蛋白修饰中标数
今天,我们继续提供一些可以参考的研究方向和思路,并在后面附上一些案例供大家参考。 探讨组蛋白乳酸化在调节细胞代谢过程中的作用,包括能量代谢、细胞增殖和分化。 研究组蛋白乳酸化在不同疾病(如癌症、炎症性疾病、神经退行性疾病、心血管疾病等)中的变化及其潜在的病理生理意义。 探索组蛋白乳酸化如何影响基因表达的调控,以及它与其他表观遗传修饰(如乙酰化、甲基化)的相互作用。 组蛋白修饰的“书写器”、“擦除器”和“阅读器”共同参与了一个复杂的调控网络,通过精细调节组蛋白的化学状态来控制基因的表达,从而影响细胞的功能和命运。
乳酸化writers:由HAT家族的p300介导乳酸化修饰,乳酸化erases:去乙酰化酶HDAC1-3和SIRT1-3则具有去乳酰化酶活性。鉴于赖氨酸酰化修饰的普遍性,乳酸化修饰中必定存在更多类型和功能的“writers”、“ereasers”和“readers”等待进一步探索,其中“readers”的相关研究仍然是一片空白。 研究组蛋白乳酸化的动态变化,包括它是如何被添加和移除的,以及这些变化在细胞周期和发育过程中的意义。 目前已报道的组蛋白乳酸化集中在人和小鼠中,其他物种比如植物、微生物则鲜有报道,即使有,但在机制上研究也不够深入。 研究组蛋白乳酸化如何参与细胞信号传导途径,以及它如何影响细胞的响应和功能。 1. 乳酸化在细胞代谢中的作用:探讨组蛋白乳酸化在调节细胞代谢过程中的作用,包括能量代谢、细胞增殖和分化在细胞代谢过程中,乳酸是糖酵解过程的最终产物之一。在氧气供应不足或细胞高度活跃(如肿瘤细胞)的情况下,乳酸的产生量会增加。乳酸可以转化为乳酰辅酶A,从而促进组蛋白的乳酸化修饰。组蛋白乳酸化作为一种代谢产物的直接反映,将细胞的代谢状态与基因调控网络连接起来,使细胞能够根据当前的代谢需求调整基因表达模式。 2024年1月2日,康奈尔大学的Marcos Simoes-Costa教授研究团队在Nature Commun(IF=16.6)发表题为“Histone lactylation couples cellular metabolism with developmental gene regulatory networks”的研究论文。该研究发现由糖酵解调控的组蛋白乳酸化将胚胎细胞的代谢状态与染色质组织和基因调控网络(GRN)激活联系起来。胚胎细胞表现出多样的代谢状态。近期研究表明,代谢重编程通过影响基因表达来驱动细胞身份的变化。然而,细胞代谢与基因表达之间的联系仍然知之甚少。考虑到糖酵解通量增加在发育过程中的重要性,该研究聚焦于乳酸化对发育基因调控网络激活的重要性。
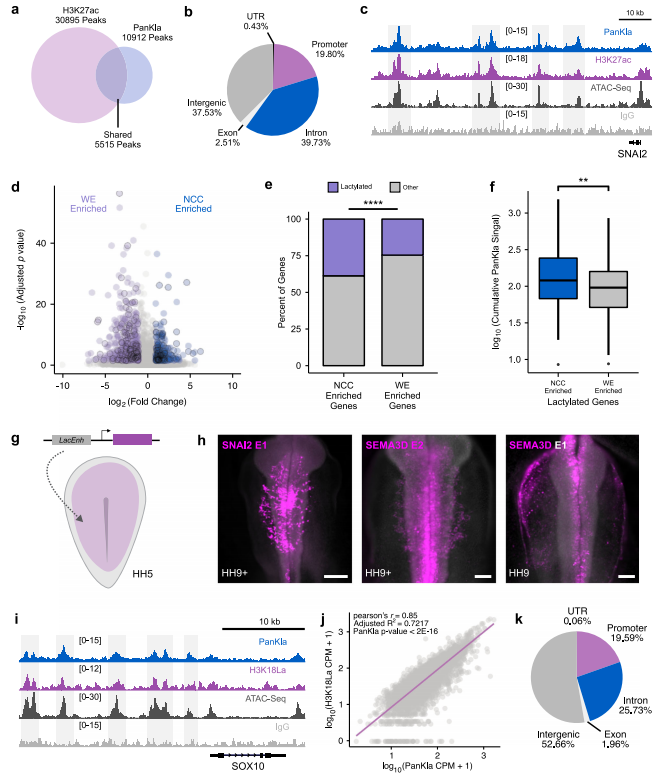
在研究中,作者使用泛抗体PanKla进行CUT&RUN,鉴定了10,912个峰,它们被定位在它们最近的注释基因上。该分析表明,乳酸化主要沉积在基因组的基因间区(42.35%),同时也沉积在内含子(34.10%)、启动子(20.78%)、外显子(2.22%)和UTR(0.55%)区域。研究团队将PanKla数据与已发表的H3K27ac CUT&RUN数据进行整合分析。将两个数据集的峰集相交,观察到大约有一半(5515/10,912)的PanKla峰与H3K27ac重叠。与所有的PanKla峰相似,PanKla+/H3K27ac+峰也主要出现在基因组的基因间区域,并包含较高的ATAC-seq信号。 为了探究乳酸化基因组位点在驱动组织特异性基因表达中的参与,研究检测了与NCC基因相关的PanKla水平峰值。作者将他们的乳酸化基因集与之前发表的NCC基因集相交,NCC基因集是比较了6个发育阶段的NCC和全胚胎(WE)细胞的基因表达数据。作者发现,与WE基因集相比,乳酸化基因(即与PanKla峰相关的基因)在NCC基因集中富集;与WE基因相比,NCC基因集中的乳酸化基因具有更高的累积PanKla信号。 为了确定乳酸化的顺式调节区域是否可以作为增强子,研究在转基因胚胎中利用报告实验检测了PanKla+/H3K27ac+峰的活性。实验结果显示PanKla标记的顺式调节元件可以作为NCC特异性增强子。研究团队从文献中收集了一个鸟类活性增强子(胚胎头部和NCC区域)的列表,并且检查它们在数据中是否有乳酸化,结果显示有68%的增强子被乳酸化了。这些结果显示,至少部分由NCCs中的乳酸化标记的顺式调控元件显示出增强子活性。这和文献报道的结果一致。因此,研究团队进行了H3K18la的CUT&RUN实验,结果发现这个组蛋白标记的水平与NCCs中的PanKla水平密切相关。此外,H3K18La峰的基因组分布与PanKla峰相似,其中大部分位于基因组的基因间区域。因此,H3K18La存在于NCCs中,并沉积在基因组的活性区域。综上所述,这些结果表明乳酸化发生在组织特异性增强子,并且标记早期发育中构成NCC特异性特征的基因。
图:乳酸化标记着活跃的组织特异性增强子。 2. 乳酸化与疾病的关联乳酸与Warburg 效应(有氧糖酵解)高度相关,另外它也参与调控肿瘤、心血管系统、呼吸系统、消化系统、泌尿系统等多个疾病,在疾病的临床诊断和预后中起着重要的作用。所以,组蛋白乳酸化疾病相关的研究也不少。比如说,在多种癌症中,组蛋白乳酸化可以通过改变基因表达模式来促进肿瘤的生长和转移。此外,乳酸化还可能影响肿瘤微环境,促进肿瘤细胞逃避免疫系统的监视。除了肿瘤,其他诸如炎症性疾病、神经退行性疾病、心血管疾病亦有报道。 2023年9月8日,浙江大学医学院附属第一医院泌尿外科研究团队王非凡、谢波医生在期刊Molecular Cancer(IF=37.3)发表文章“CircXRN2 suppresses tumor progression driven by histone lactylation through activating the Hippo pathway in human bladder cancer”。该研究旨在探索循环RNA(circRNA)在人类膀胱癌中的作用和分子机制,发现circXRN2通过LATS1激活了Hippo信号通路,从而抑制膀胱癌中由H3K18乳酸化介导的肿瘤进展。
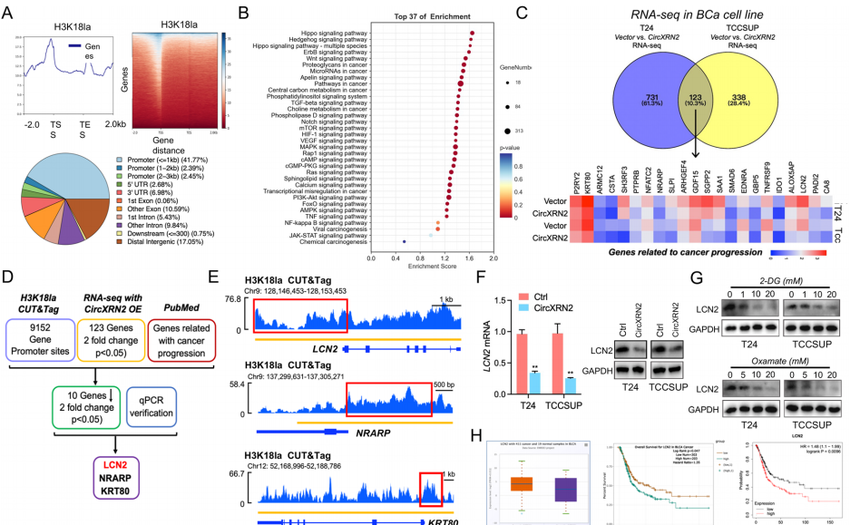
为了阐释H3K18la的调控机制,研究使用CUT&Tag技术对T24细胞进行分析。研究结果显示H3K18la在大量基因的启动子区域富集。KEGG富集分析显示H3K18la关联基因主要富集于调控肿瘤发生的多个信号通路,表明H3K18la修饰在人膀胱癌进展中的关键作用。然后,研究进行RNA-seq,并将其与CUT&Tag数据进行关联分析,同时结合PubMed数据库,用qPCR验证找到3个候选基因:LCN2、NRARP和KRT80。作者在circXRN2过表达的细胞中验证了上述靶点在mRNA水平上的表达,结果显示LCN2可以被circXRN2显著调控。在过表达circXRN2的T24和TCCSUP细胞中,检测了LCN2 mRNA和LCN2蛋白的表达水平。结果显示,circXRN2显著下调了LCN2。此外,糖酵解抑制剂也在蛋白水平上调节了LCN2的表达。最近,LCN2被确定为癌症进展的促进剂。作者在TCGA数据库和Kaplan-Meier Plotter数据库中,发现LCN2在膀胱癌组织中表达上调,并与膀胱癌进展密切相关。 基于上述证据,作者选择LCN2进行以下研究。根据之前的CUT&Tag测序,作者设计了针对LCN2启动子不同区域的特异性引物,ChIP检测显示H3K18la在LCN2启动子中富集。糖酵解抑制剂和circXRN2可以减少H3K18la和LCN2启动子之间的相互作用,进一步表明H3K18la在LCN2转录中的关键作用。
图:LCN2是H3K18乳酸化的靶基因,并且充当癌基因的作用。 3. 乳酸化与表观遗传调控探索组蛋白乳酸化如何影响基因表达的调控,以及它与其他表观遗传修饰(如乙酰化、甲基化)的相互作用。表观遗传调控涉及的机制有DNA&RNA修饰、组蛋白修饰、染色质可及性以及非编码RNA,上一个案例呈现的就是非编码RNA与组蛋白乳酸化H3K18la的调控关系。其实,目前已报道的研究中,有不少将乳酸化与表观修饰关联的思路。往期我们分享过一些文章解读,研究中都有将H3K18la与组蛋白乙酰化、组蛋白甲基化修饰进行比较分析。 目前,已发表文章中有一些与RNA甲基化修饰相关联的案例。2021年,上海交通大学医学院的研究团队在Genome Biology(IF=12.3)发表题为“Histone lactylation drives oncogenesis by facilitating m6A reader protein YTHDF2 expression in ocular melanoma”的研究论文。该研究以黑色素瘤为研究对象,发现组织黑色素瘤中组织乳酸化水平升高,并与预后不良相关。在机制上,组织乳酸化通过促进m6A阅读蛋白YTHDF2的表达促进了肿瘤发生。此外,YTHDF2识别m6A修饰的PER1和TP53 mRNA,从而参与了组织乳酸化在组织黑色素瘤中的作用。研究还揭示了组织乳酸化和m6A甲基化在组织黑色素瘤中的相互作用。
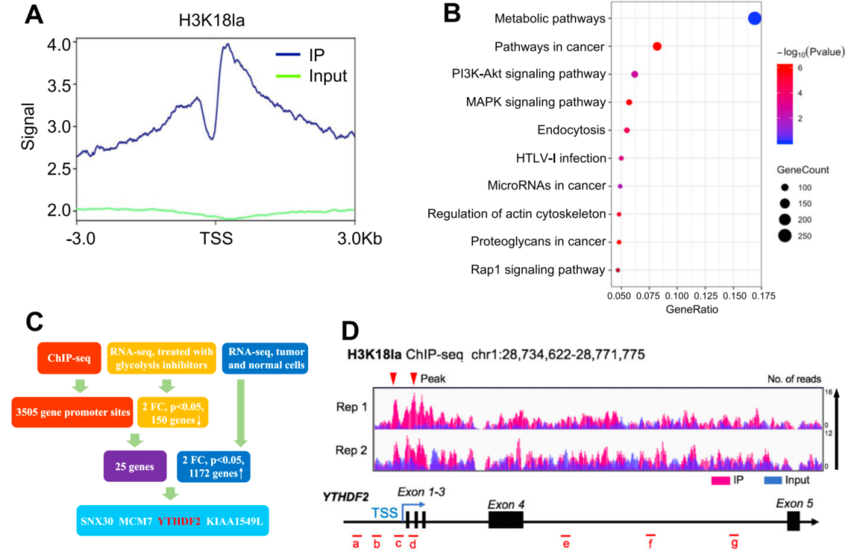
为了揭示组蛋白乳酸化在基因表达中的调控作用,研究团队首先进行了染色质免疫共沉淀,然后使用抗H3K18la抗体进行测序(ChIP-seq),研究结果显示H3K18la在启动子区域富集。KEGG富集分析发现这些H3K18la特异性基因在代谢途径和肿瘤相关途径中富集,提示组蛋白乳酸化在肿瘤发生中的调节作用。将ChIP-seq数据与RNA-seq数据(用糖酵解抑制剂处理或未处理)关联,他们鉴定到在糖酵解抑制剂处理的细胞中mRNA水平显著降低,并且在肿瘤细胞中也高表达的 4 个靶基因。 在这些候选基因中有一个YTHDF2蛋白,是m6A的阅读器之一,已被报道在几种肿瘤中作为致癌基因。研究团队聚焦于该基因,为了证实YTHDF2的转录是被H3K18la激活的,通过ChIP-seq数据的peak可视化图可以观察到YTHDF2启动子上的H3K18la信号的显著富集。ChIP-qPCR检测也表明,H3K18la在YTHDF2启动子区域富集,而糖酵解抑制剂降低了这种富集。 此外,ChIPqPCR检测显示,经糖酵解抑制剂处理后,组蛋白乳酸化writer蛋白EP300在YTHDF2启动子上的结合水平显著降低。然而,在YTHDF2缺失的细胞中,EP300的整体蛋白表达保持不变。值得注意的是,在此条件下,YTHDF2启动子的H3K27ac水平略有下降。正如预期,在糖酵解抑制剂处理的细胞中YTHDF2的mRNA和蛋白表达水平显著减少。此外,mRNA稳定性分析表明,糖酵解抑制剂并不影响YTHDF2的mRNA稳定性。在黑色素瘤中,YTHDF2与整体组蛋白乳酸化和H3K18la的水平正相关。总体来说,YTHDF2受到H3K18la的正调控。
图:组蛋白乳化激活了YTHDF2的转录 4. 新物种中组蛋白乳酸化的鉴定和机制研究2023 年,北京市农林科学院玉米研究所在期刊Science China Life Sciences发表题为“Trash to treasure: lactate and protein lactylation in maize root impacts response to drought”的研究论文。在此研究前,关于植物组织中是否存在生物活性乳酸的共识争论尚未得到解决,如果存在,其通过翻译后修饰的潜在调控功能尚未见报道。该研究反复鉴定了干旱胁迫下玉米根系组织中的乳酸,并证明了组蛋白和非组蛋白乳酸化在玉米品系中普遍存在(干旱敏感和耐受)。
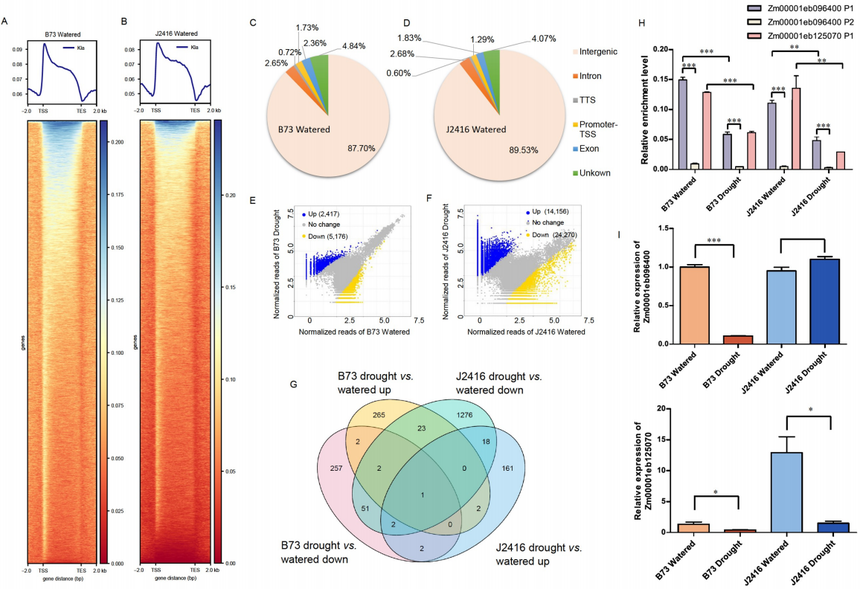
研究在组蛋白上发现37个Kla位点,研究团队利用泛抗Kla抗体进行ChIP-Seq分析,进一步探讨了组蛋白Kla标记在玉米根系中的全基因组分布。在浇水的B73和J2416中分别鉴定到28,942(2160个基因)和48,774(3121个基因)Kla峰。这两个品系都展现出类似的组蛋白Kla修饰模式,信号在TSS的上游被耗尽,在TSS周围富集,随着信号逐渐减少,直到TES。近90%的组蛋白Kla峰与基因间区域相关,只有大约6%的信号出现在基因区域。研究结果表明,组蛋白Kla可能是一种独特的标记,可能有助于染色质结构的调控,因为它广泛分布于基因间区域。干旱处理改变了两个品系的组蛋白乳酸化信号,B73品系显示2417个上调和5176个下调峰,J2416品系显示14156个上调和24270个下调峰。差异Peak关联基因分析显示在B73和J2416两个品系中有58个基因有相同的模式,在所有差异标记基因中仅占比2.7%。这些结果表明,组蛋白Kla调控在干旱两种品系之间是不同的。 目前还不清楚组蛋白Kla标记是如何调控的,以及它如何影响植物的基因表达,但已在动物中证明Kla正向调控糖酵解和稳态基因的表达。Zm00001eb096400编码一种卵磷脂-胆固醇酰基转移酶,在干旱处理的B73中下调峰最多(5个),RNA-seq数据表明与浇水的B73相比,该基因的表达显著降低。相比之下,在J2416中只发现了一个下调的峰,而转录水平没有变化。此外,在干旱胁迫下,J2416中Zm00001eb125070中有3个峰值表达下调,这与其表达水平的下调相一致。通过ChIP-qPCR和qPCR验证了这些结果。综上所述,组蛋白Kla在玉米基因组中普遍存在,在外界胁迫中高度动态,似乎与基因激活有关。
图:玉米组蛋白Kla标记的全基因组图谱。 今天我们分享了组蛋白乳酸化的一些研究方向和案例,爱基百客作为领先的表观组学服务商,可以提供包含ChIP-seq、CUT&Tag、ATAC-seq、WGBS、ncRNA测序、scRNA-seq和scATAC-seq等技术服务,欢迎各位老师咨询。此外,我们也针对组蛋白修饰方向提供了一个可行性方案,感兴趣的老师可以联系销售获取~ [1] Qu J, Li P and Sun Z (2023) Histone lactylation regulates cancer progression by reshaping the tumor microenvironment.Front.Immunol.
项目咨询 了 解 更 多 { 往 期 精 彩 回 顾 } 精选合集,欢迎收藏哟! |