NEWS
新闻资讯
|
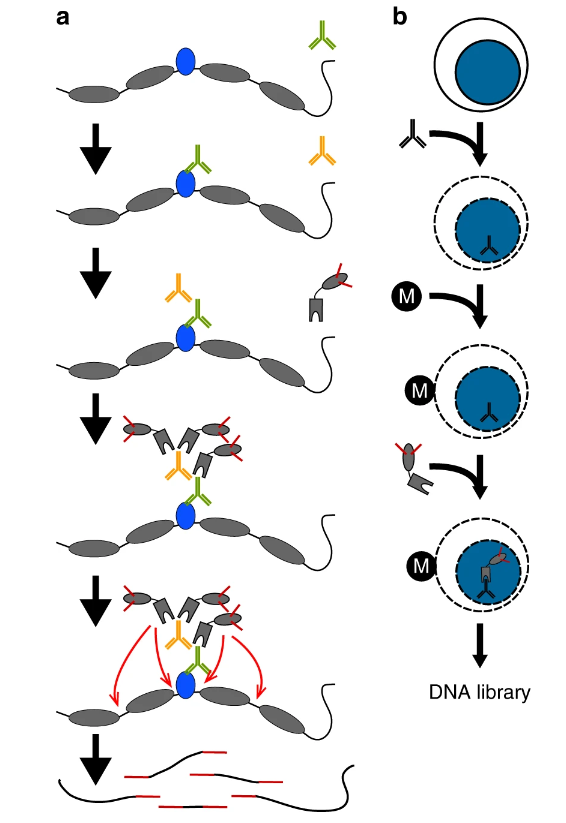
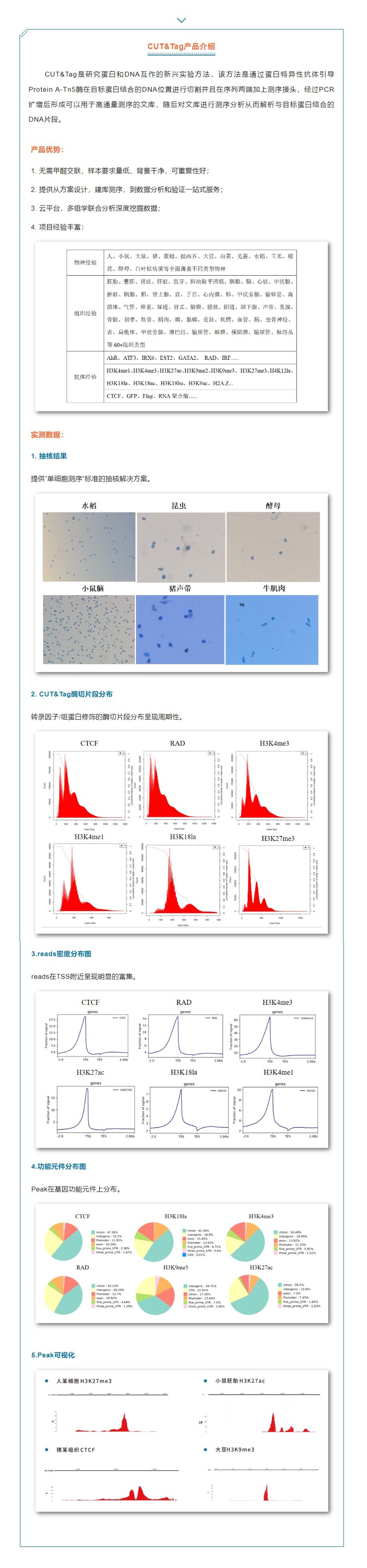
CUT&Tag与ATAC-seq联手,解析表观遗传机制CUT&Tag:CUT&Tag是研究蛋白和DNA互作新兴的实验方法,该方法是通过蛋白特异性抗体引导Protein A-Tn5酶精确切割目标蛋白结合的DNA区域,并在这些序列的两端加上测序接头,经过PCR扩增后形成可用于高通量测序的文库,随后对文库进行测序分析从而解析与目标蛋白结合的DNA片段。CUT&Tag技术可以在单个细胞水平上进行高分辨率的蛋白-染色质相互作用研究,适用于低丰度蛋白的检测。常用于研究组蛋白修饰、转录因子结合位点和转录辅因子等。此外,CUT&Tag技术也适用于探究非典型DNA结构,如G-四链体(G4),这对于理解基因调控和疾病发生具有重要意义。
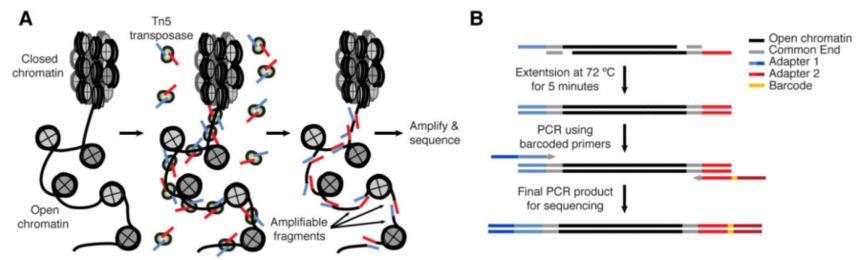
Fig1.CUT&Tag原理[1] ATAC-seq:ATAC-seq(Assay for Transposase-Accessible Chromatin using sequencing)是一种用于研究染色质可及性的高通量测序技术。它利用转座酶Tn5的特性,识别并切割开放的染色质区域,同时将测序接头插入到这些区域。通过这种方法,ATAC-seq技术可以快速、高效地映射基因组的开放区域和调控元件,适用于研究基因表达调控和表观遗传学。ATAC-seq广泛应用于研究启动子、增强子和其他调控元件的开放性变化,以及细胞类型特异性的染色质结构。
Fig2.ATAC-seq原理[2] 两种方法都使用了Tn5酶进行染色质处理,都是染色质学技术,用于研究基因组结构和调控,能够提供关于基因表达调控的信息。然而,它们在研究重点和操作流程上存在一些区别: 1)CUT&Tag更侧重于蛋白-染色质相互作用的研究,可以提供更详细的蛋白-染色质相互作用信息,有助于深入理解蛋白在基因调控中的具体作用机制;而ATAC-seq则主要专注于研究染色质的开放性,即哪些区域对转录因子和其他调控蛋白是可及的,它可以用于研究基因调控网络、细胞类型特异性的染色质状态以及疾病状态下的表观遗传变化。 2)CUT&Tag通常需要特定抗体对蛋白进行标记,而ATAC-seq则只需要通过酶切来检测开放的染色质区域。 目前越来越多的研究将CUT&Tag和ATAC-seq进行了联合应用,它们能够互补地提供关于染色质状态和蛋白质-DNA相互作用的全面信息。前面的文章我们分享了《scATAC-seq+CUT&Tag探究关键转录因子对视网膜细胞分化的调控作用》,今天我们来看一下CUT&Tag与bulk ATAC-seq联手,是如何解析表观遗传机制。 案例一:CUT&Tag+ATAC-seq揭示2型糖尿病中STING调控葡萄糖稳态的关键转录因子[3]
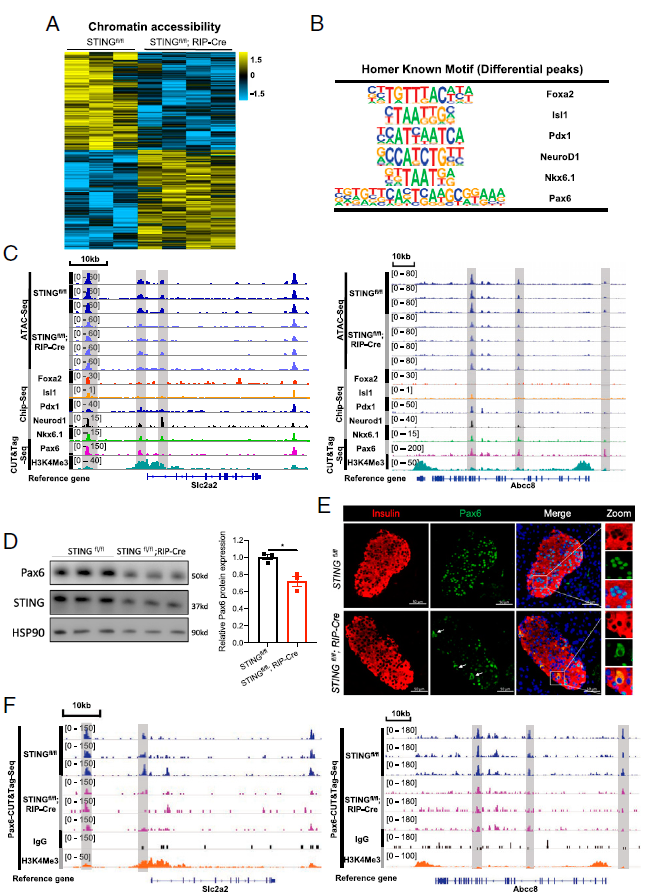
本研究探讨了STING(刺激干扰素基因的因子)在2型糖尿病(T2D)中胰岛素抵抗和β细胞功能障碍的分子基础上的作用。研究者们使用global STING knockout (STING-/-)和β-cell–specifific STING knockout (STING-βKO) 小鼠模型,揭示了STING在通过外周组织和β细胞调节葡萄糖稳态中的不同作用。胰岛转录组分析显示,STING缺乏降低了与β细胞功能相关的基因表达,包括Glut2、Kcnj11和Abcc8,导致GSIS受损。在机制上,ATAC-seq和CUT&Tag分析表明Pax6可能是与STING-βKO小鼠中缺陷GSIS相关的转录因子。实际上,STING-βKO β细胞中Pax6的mRNA和蛋白质水平下调,其核定位丧失。这些数据揭示了STING在调节胰岛素分泌中的功能,并确立了β细胞和胰岛素靶组织中精细调节的STING在维持葡萄糖稳态中的病理生理意义。
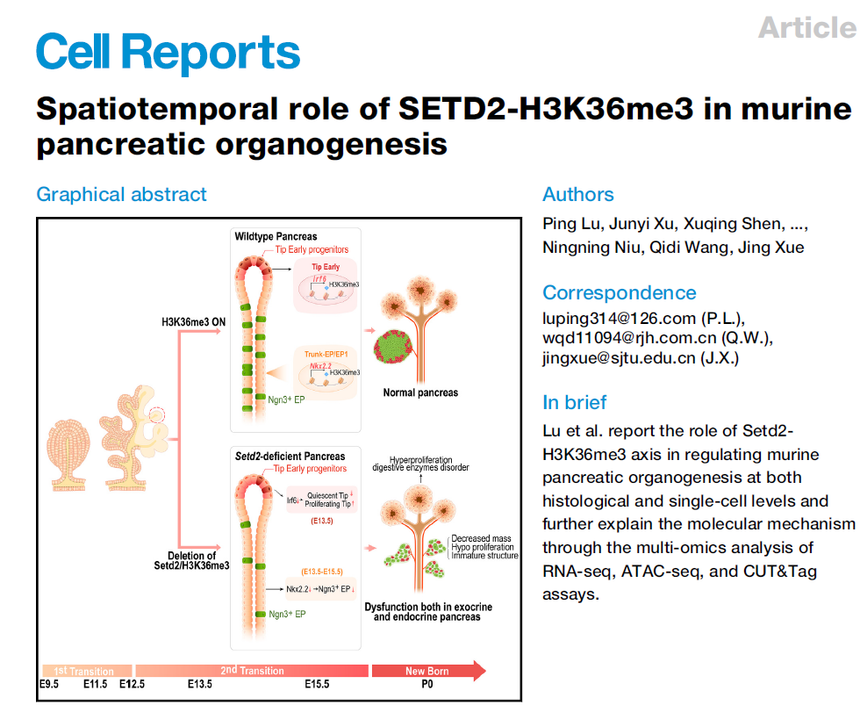
Fig3.Pax6是与STING-β KO小鼠GSIS缺陷相关的关键转录因子 案例二:CUT&Tag+ATAC-seq揭示SETD2-H3K36me3在小鼠胰腺器官形成中的时空作用[4]
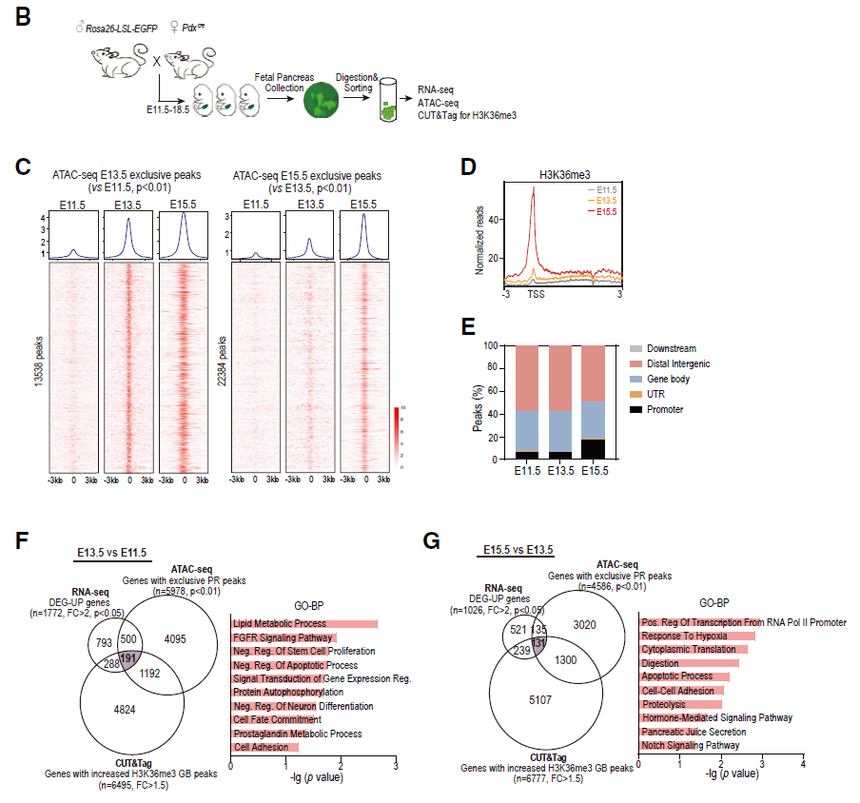
本研究探讨了SETD2(H3K36me3的主要组蛋白甲基转移酶)在胰腺发育中的作用。尽管已有多年研究,但关于组蛋白修饰如何协调胰腺发育的机制仍存在许多未知。研究者们结合CUT&Tag、ATAC-seq和RNA-seq技术,发现从次过渡阶段开始H3K36me3水平显著增加,并解析了相关的转录变化。通过scRNA-seq,研究定义了Setd2在胰腺特异性敲除后,导致外分泌和内分泌谱系的异常:过度增殖的尖端祖细胞导致异常分化;Ngn3+内分泌祖细胞因Nkx2.2下调而减少,导致内分泌发育不足。这些数据确定了SETD2在胚胎胰腺发育中的关键作用,并为理解胰腺疾病中组蛋白修饰失调提供了线索。
Fig4. 胰腺器官发生过程中动态H3K36me3水平和相关转录组谱 案例三:CUT&Tag+ATAC-seq揭示植物精细胞命运决定的表观遗传调控机制[5]
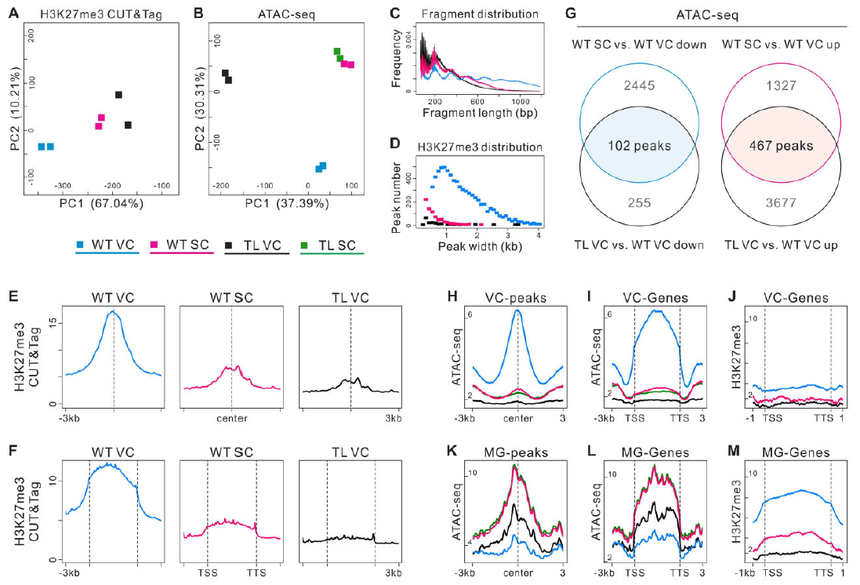
本研究揭示了H3K27甲基化在拟南芥雄性配子体中营养细胞(VC)和雄性生殖系(MG)命运决定中的关键作用。通过遗传转化技术创建特异性擦除VC中H3K27me3的转基因拟南芥系(TL),并观察到这种擦除扰乱了VC的正常发育,导致其命运向MG细胞转变。CUT&Tag、ATAC-Seq和RNA-Seq等组学联合分析进一步揭示了擦除营养细胞中的H3K27me3可以导致其染色质重塑,并激活精细胞分化所必需的特异基因转录,诱导了细胞命运的转变。透射电子显微镜观察进一步证实了VC向MG细胞超微结构的转变。研究结果表明,H3K27甲基化是调控植物雄性生殖发育的表观遗传开关,对花粉育性至关重要。
Fig5.H3K27me3的消除导致TL VC染色质重塑 ATAC-seq数据可以得到染色质开放性的动态变化,联合CUT&Tag可以进一步探究调控某一生物学过程的关键因子(包括顺式调控元件和转录因子等),这种联合分析还可以揭示表观遗传修饰如何影响转录因子的结合和活性,从而为疾病发生、发展以及治疗提供新的分子机制和潜在的治疗靶点。 爱基百客拥有10年表观遗传学研究服务的经验,我们的表观组学和单细胞测序平台技术已十分完善。我们提供从大规模(Bulk级别)的CUT&Tag、ATAC-seq、ChIP-seq到单细胞级别的scATAC-seq、scChIP-seq等一系列高精度的表观遗传学测序服务。我们的服务范围涵盖实验设计、样本处理、数据分析到验证的全流程,旨在为客户提供全面、专业的技术支持。如果您在表观遗传学研究领域有任何技术需求,欢迎随时联系我们,我们期待为您的科研工作助力!
项目咨询
参考文献: 1. Kaya-Okur H S, Wu S J, Codomo C A, et al. CUT&Tag for efficient epigenomic profiling of small samples and single cells[J]. Nature communications, 2019, 10(1): 1930. 2. Buenrostro J D, Giresi P G, Zaba L C, et al. Transposition of native chromatin for fast and sensitive epigenomic profiling of open chromatin, DNA-binding proteins and nucleosome position[J]. Nature methods, 2013, 10(12): 1213-1218. 3. Qiao J, Zhang Z, Ji S, et al. A distinct role of STING in regulating glucose homeostasis through insulin sensitivity and insulin secretion[J]. Proceedings of the National Academy of Sciences, 2022, 119(7): e2101848119. 4.Lu P, Xu J, Shen X, et al. Spatiotemporal role of SETD2-H3K36me3 in murine pancreatic organogenesis[J]. Cell Reports, 2024, 43(2). 5. Huang X, Sun M X. H3K27 methylation regulates the fate of two cell lineages in male gametophytes[J]. The Plant Cell, 2022, 34(8): 2989-3005. 了 解 更 多 { 往 期 精 彩 回 顾 } 精选合集,欢迎收藏哟!
|